实验室用标准盐酸测定NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏低的是( )
| A.酸式滴定管在装酸液前未用标准盐酸溶液润洗2~3次 |
| B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 |
| C.锥形瓶内溶液颜色由黄色变橙色,立即记下滴定管内液面所在刻度 |
| D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 |
硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发展水平的一种标志。目前的重要生产方法是“接触法”,有关接触氧化反应 2SO2+O2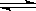 2SO3的说法不正确的是 ( )
2SO3的说法不正确的是 ( )
| A.该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫 |
| B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零 |
| C.一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等 |
| D.在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 |
下列关于甲烷分子结构的叙述中,正确的是 ( )
A.甲烷分子中C、H原子间是离子键 B.甲烷分子的空间结构是正方体
C.甲烷的结构式为CH4 D.甲烷分子中4个碳氢键完全相同
废电池必须进行集中处理的首要原因是 ( )
| A.充电后可再使用 |
| B.回收利用石墨电极和金属材料 |
| C.防止电池中汞、镉和铅等重金属离子污染土壤和水源 |
| D.防止电池中的电解质溶液腐蚀其他物品 |
下列属于吸热反应的是 ( )
| A.金属钠与水的反应 | B.氢气燃烧 |
| C.浓硫酸的稀释 | D.Ba(OH)2·8H2O和NH4Cl(固体)混合 |
在元素周期表中金属与非金属的分界处,可以找到 ( )
| A.合金 | B.半导体材料 | C.催化剂 | D.农药 |