有A、B、C、D、E、F六种短周期元素,它们的核电荷数按C、F、A、B、D、E的顺序增大。已知E、F位于同一主族;C、D都能分别与A按原子个数比为1∶1 或2∶1形成化合物;CB是一种10e- 的气态分子;E的M层电子数是K层电子数的2倍。
(1)写出下列元素的名称:B ,E ,F ;
(2)写出E在元素周期表中的位置第 周期第 族;
(3)写出D2A2的电子式 ;EB4
(4)用电子式表示FA2的形成过程 ;
(5)比较元素E和F的非金属性强弱,E的非金属性 于F(填“强”或“弱”),并用化学方程式证明上述结论 ;
(6)以上A、B、C、D中某些元素可形成的既含离子键又含非极性共价键的化合物是 ;既含离子键又含极性共价键的化合物是 。(写化学式)
在Cu+2H2SO4(浓) CuSO4 +SO2↑+2H2O 反应中,
CuSO4 +SO2↑+2H2O 反应中, 是氧化剂,还原剂是,元素被氧化,是还原产物,电子转移的总数为。
是氧化剂,还原剂是,元素被氧化,是还原产物,电子转移的总数为。
有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。请回答下列问题:
(1)E的化学式是_________________________
(2)反应①的离子方程式为
(3)写出另外一种实验室制取H的化学方程式
(4)反应②的化学方程式为
将Cu投入足量的FeCl3的水溶液中,两者发生反应的化学方程式如下
2FeCl3+Cu= 2FeCl2+CuCl2
(1)请用双线桥法标出电子转移的方向和数目。
(2)在该反应中,氧化剂是___________,氧化产物是___________。
(3)当有0.3mol电子发生转移时,发生反应的Cu的质量为___________g。
(4)请将以上反应改写为离子方程式_______________________________。
在自然界中许多元素有多种核素,如氧元素存在 、
、 、
、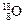 三种核素,氢元素有
三种核素,氢元素有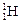 、
、 、
、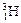 三种核素。
三种核素。
(1) 、
、 、
、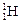 、
、 四种核数最多可以组成种水
四种核数最多可以组成种水 分子
分子
(2)现有11g由 和
和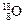 组成的水分子,其中含中子数为mol,电子数为个。
组成的水分子,其中含中子数为mol,电子数为个。
(3)请画出 2—微粒的结构示意图:。
2—微粒的结构示意图:。
下列物质:①H2O ②石墨 ③NH4NO3④液态氯化氢⑤冰醋酸 ⑥蔗糖
属于强电解质的是;属于弱电解质的是;属于非电解质的是(用编号填写)。