实验室常用CuSO4溶液吸收H2S气体:CuSO4+H2S ® CuS¯+H2SO4,由该反应不能推测
| A.一定条件下弱酸可以制强酸 | B.饱和溶液中H2S比CuS提供的S2-浓度大 |
| C.CuS不溶于硫酸 | D.反应FeSO4+H2S ® FeS¯+H2SO4也能发生 |
从下列反应物到下列生成物,反应类型可能属于消去反应的是()
A. |
B.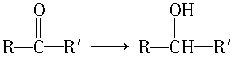 |
| C.R—X→ROH |
D. |
下列有机物沸点最高的是()
| A.乙烷 | B.氯乙烷 | C.1-氯丙烷 | D.1-氯丁烷 |
下列关于卤代烃的叙述中正确的是()
| A.所有卤代烃都是难溶于水,比水重的液体 |
| B.所有卤代烃在适当条件下都能发生消去反应 |
| C.所有卤代烃都含有卤原子 |
| D.所有卤代烃都是通过取代反应制得的 |
已知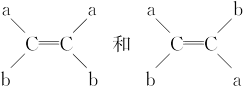 (a,b为不同的原子或原子团)互为同分异构体,称为烯烃的顺反异构。试推断一氯丙烯的同分异构体(不含环状结构)共有( )
(a,b为不同的原子或原子团)互为同分异构体,称为烯烃的顺反异构。试推断一氯丙烯的同分异构体(不含环状结构)共有( )
| A.3种 | B.4种 | C.5种 | D.6种 |
医学上在对抗癌物质的研究中发现 具有抗癌作用,而
具有抗癌作用,而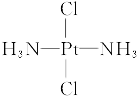 没有抗癌作用。对此下列有关叙述正确的是( )
没有抗癌作用。对此下列有关叙述正确的是( )
| A.两者互为同分异构体,都是以Pt原子为中心的四面体结构 |
| B.两者互为同分异构体,都是以Pt原子为中心的平面结构 |
| C.两者为同一物质,都是以Pt原子为中心的四面体结构 |
| D.两者为同一物质,都是以Pt原子为中心的平面结构 |