某化学兴趣小组的同学设计了一套实验方案探究元素周期表中元素性质的变化规律;同一周期内从左到右元素金属性的递变规律;同一主族内从上到下元素非金属的递变规律。
| 实验方法(Ⅰ) |
实验现象(Ⅱ) |
| 1、钠与冷水反应 |
a、溶液变红色 |
| 2、向NaOH溶液中滴加酚酞 |
b、产生白烟 |
| 3、向新制H2S饱和溶液滴加新制的氯水 |
c、反应不十分剧烈,产生的气体能燃烧,溶液变成浅红色。与酸反应剧烈,产生大量气泡且可以燃烧 |
| 4、镁带在空气中燃烧 |
d、产生大量气泡、气体可以燃烧 |
| 5、NaI溶液中加入溴水和CCl4 |
e、下层溶液变橙色 |
| 6、镁带与沸水反应,再向反应后溶液中滴加酚酞。镁与2mol/L盐酸反应。 |
f、浮于水面,熔成小球,迅速向四处游动 |
| 7、蘸浓氨水与浓盐酸的两玻璃棒接近 |
g、下层溶液变紫色 |
| 8、NaBr溶液中加入氯水和CCl4 |
h、发出耀眼的强光,生成白色物质 |
| 9、铝片与2mnol/L盐酸反应 |
i、生成淡黄色沉淀 |
回答下列问题
(1)从上表(Ⅰ)中选择实验方法,从(Ⅱ)中选择相应的实验现象,上下对应地填写符合要求的答案在空格中(有几个填几个,不一定把空格填满)。
| |
1、探究同一周期从左到右元素金属性的递变规律 |
2、探究同一主族内从上到下元素非金属性的递变规律 |
||||||
| Ⅰ |
|
|
|
|
|
|
|
|
| Ⅱ |
|
|
|
|
|
|
|
|
(2)实验结论(表示元素具体的强弱顺序):
金属性:____________________ 非金属性:
(3)上表(Ⅰ)中实验方法9反应的离子方程式
(4)上表(Ⅱ)中实验现象e反应的离子方程式
铁砂的主要成分是微粒状的磁性氧化铁、石英、石灰石等混合物。某化学兴趣小组从铁砂中分离出磁性氧化铁,并进行铝热反应实验。
(1)取磁性氧化铁按图中甲装置进行铝热反应,现象很壮观。取少许反应生成的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现这种结果的原因,除了可能混有没反应的磁性氧化铁外,还有一个原因是。
(2)为了克服图中甲的缺陷,改用图中乙装置进行铝热反应,主要步骤如下:
①在一个广口容器中放进一定量的干燥细沙;
②将一定量的铁砂和铝粉混合物装在纸漏斗中并埋入细沙里;
③将一定量的镁粉和氯酸钾混合物放在铝热剂上;
④再放上引火剂;引火反应,冷却;⑤取出反应后的铁块(如图丙)
请写出铝热反应的化学方程式:
取少许反应生成的铁块溶于盐酸,向其中滴加KSCN溶液,溶液没有出现血红色。实验中干燥细沙的主要作用是。
(3)测定图中乙反应所得的铁块纯度,流程如下图所示。几种氢氧化物开始沉淀和沉淀完全时的pH参考19题。
①试剂A应选择,试剂B应选择。
| A.稀盐酸 | B.氧化铁 | C.H2O2溶液 | D.氨水 E.MgCO3固体 |
②操作Ⅰ的名称为。操作Ⅱ的名称为。固体M完全转化为固体N的标志是。
③已知常温下Fe(OH)3的KSP=4.0×10-38,求反应Ⅲ后溶液中c(Fe3+)=mol/L
④若最终红色粉末质量为14.14g,则该铁块的纯度是。如果直接洗涤、烘干和称量固体M的质量,计算铁块的纯度,则计算结果会(填“偏大”“偏小”或“无影响“)。原因是。
某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。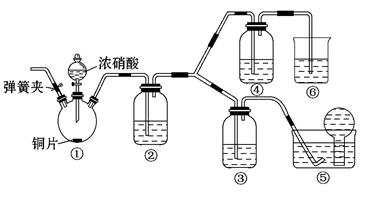
可选药品:浓硝酸、3 mol·L-1稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳。
已知:氢氧化钠溶液不与NO反应,能与NO2反应:
2NO2+2NaOH====NaNO2+NaNO3+H2O
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是
。
(2)滴加浓硝酸之前的操作是检验装置的气密性,加入药品,打开弹簧夹后
。
(3)装置①中发生反应的化学方程式是
。
(4)装置②的作用是 ,
发生反应的化学方程式是
。
(5)该小组得出结论的实验现象是
。
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是 (选填序号字母)。
a.加热该绿色溶液,观察颜色变化
b.加水稀释绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
资料显示:“氨气可在纯氧中安静燃烧……”。某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。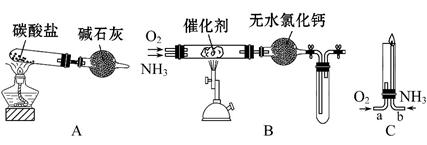
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是 ;碱石灰的作用是 。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热。氨催化氧化的化学方程式是;
试管内气体变为红棕色,该反应的化学方程式是
。
(3)将过量的氧气与A产生的氨气分别由a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是 ,
其理由是 。
②氨气燃烧的化学方程式是 。
某同学用下列装置(固定、加热仪器和橡胶管略)进行有关氨气制取的实验探究,回答下列问题。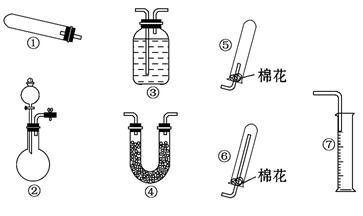
(1)若用装置①制取NH3,其反应的化学方程式为
;
若要测定生成的NH3的体积,则必须选择的装置是 (填装置序号),装置中所盛试剂应具有的性质是 。
(2)若用装置②制取并收集干燥的NH3,烧瓶内装的试剂是 ,分液漏斗中装的试剂是 ,收集装置应选择 (填装置序号)。证明氨气已收集满的操作是 。检验装置②的气密性的方法是 。
已知:Cu+4HNO3(浓)====Cu(NO3)2+2NO2↑+2H2O。为探究如何尽可能多地使NO2被水吸收,某活动小组设计并完成了以下实验。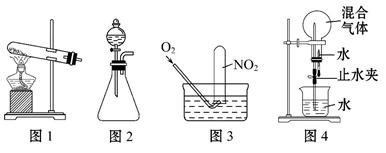
(1)活动小组同学利用铜与浓硝酸反应制取NO2、过氧化氢溶液与MnO2制取O2。
①根据反应原理他们选用了相同的装置 (填“图1”或“图2”)分别制取NO2和O2。
②写出铜与浓硝酸反应的离子方程式 。
③过氧化氢溶液与MnO2制取O2时,MnO2的作用是
_________________________________________________________________。
④收集NO2可采用的方法是 。
(2)活动小组的同学做了如下准备:用气囊收集好纯净的O2;收集了一试管NO2;用干燥的烧瓶收集了一定比例的NO2和O2混合气体。
①为了尽可能多地使NO2被水吸收,并达到较好的实验效果,利用图3吸收气体时,用气囊通入O2与直接利用制气装置制取并通入O2相比,其优点是
。
②利用图4吸收气体时,其操作和现象为
。
③NO2、O2、H2O反应的产物为硝酸,反应中NO2和O2物质的量之比a∶b= ;标准状况下,若图4中混合气体NO2和O2比例为a∶b,当混合气体全部被吸收时所得溶液物质的量浓度为 mol·L-1(保留两位有效数字)。