按已知的原子结构规律,82号元素X应是第___________周期___________族元素,它的最高正价氧化物的化学式为______________。
安徽凹山铁矿坐落在马鞍山境内,矿床属于陆相火山一侵入岩型铁矿床,俗称“玢岩型”铁矿,是马钢重要的矿区之一。铁矿中被称为红帘石的铁矿含锰量高,锰是冶炼锰钢的重要原料。红帘石主要成分有磁铁矿Fe3O4、菱铁矿FeCO3、锰矿(MnO2和MnCO3)石棉Mg3Si3O7(OH)4等。工业上将红帘石处理后运用阴离子膜电解法的新技术提取金属锰并制的绿色高效水处理剂(K2FeO4)。工业流程如下:
(1)工业上为提高稀硫酸浸取效率一般采取的措施是(任意写两种方法)
①②
(2)石棉化学式为Mg3Si3O7(OH)4也可以表示成氧化物形式,氧化物表达式为。
(3)已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
| 离子 |
Fe3+ |
Al3+ |
Fe2+ |
Mn2+ |
Mg2+ |
| 开始沉淀的pH |
2.7 |
3.7 |
7.0 |
7.8 |
9.3 |
| 完全沉淀的pH |
3.7 |
4.7 |
9.6 |
9.8 |
10.8 |
过程②中加氨水调节溶液的pH等于6,则滤渣B的成分。
(4)浸出液中以Mn2+形式存在,且滤渣A中无MnO2原因。
(5)电解装置中箭头表示溶液中阴离子移动的方向;则A电极是直流电源的极。实际生产中,阳极以稀硫酸为电解液,阳极的电极反应式为。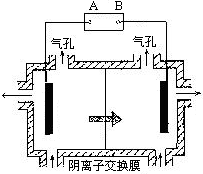
(6)滤渣经反应④生成绿色高效水处理剂的离子方程式。
K2FeO4被誉为绿色高效水处理剂的原因是。
山梨酸是一种常用的食品防腐剂,以下是山梨酸的一种工业合成途径:
|

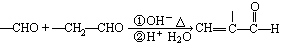
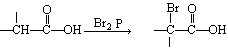

A、B、C、X、Y、Z元素的原子序数依次增大,根据信息完成问题:
| 元素A |
各能级上的电子数相等 |
| 元素C |
某种核素原子的质量数为18,中子数为10 |
| 元素X |
单质是良好的半导体材料 |
| 元素Y |
其单质为淡黄色晶体,常用来处理打碎的水银温度计 |
| 元素Z |
3d能级上有4个未成对电子 |
(1)Z元素在周期表中的位置,其电子排布式。
(2)AO2的熔点远低于XO2熔点的主要原因是。
(3)X的氧化物和NaOH溶液反应的化学方程式。
(4)B、C气态基态原子的第一电离能的大小关系为。
(5)请用离子方程式表达Na2Y溶液呈碱性的原因。
(6)已知CH3COOH(aq) H+(aq)+CH3COO—(aq)△H=+akJ/mol
H+(aq)+CH3COO—(aq)△H=+akJ/mol
CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l)△H=—bkJ/mol
则中和热的△H=kJ/mol
铅蓄电池是最常用的化学电源,它在放电、充电时的电池反应为:
试回答:
(1)铅蓄电池负极的电极材料是_______。
(2)工作时铅蓄电池正极的电极反应是___________。
(3)铅蓄电池工作过程中,电解质溶液的密度会_______(填“减小”“增大”或“不变”,下同),pH________。
(4)该铅蓄电池在充电时阳极的电极反应是___________。
(5)如果用铅蓄电池做电源电解饱和食盐水制取Cl2,已知某铅蓄电池中硫酸溶液的体积为0.8L,电解前硫酸溶液浓度为4.5mol.L-1,当制得26.88LCl2时(指在标准状况下),求理论上电解后电池中硫酸溶液的浓度为(假设电解前后硫酸溶液的体积不变)________ mol.L-1。
用下图所示装置进行实验(夹持装置已略去)。请回答下列问题:
(1)若A中为浓硝酸,B中为铜单质,C中为氢氧化钠溶液。现将浓硝酸滴入B中,则B中发生反应的化学方程式为。
(2)若A中为浓氨水,B中为生石灰,C中为明矾溶液。
①将浓氨水逐滴滴入B中,可产生大量氨气,原因可能是 _(填序号)。
a.生石灰和浓氨水反应产生氨气,氨气易溶于水
b.生石灰和水反应,消耗水,使氨气的溶解量减少
c.反应放出大量热,使氨气在水中溶解度明显降低
② C中通入过量氨气时,反应的离子方程式为。
(3)若A中为水,B中为过氧化钠,C中为酸性淀粉碘化钾溶液,将水滴入B中后,B中的实验现象为;若C中溶液变为蓝色,则C中发生反应的离子方程式为_。