下表为元素周期表的一部分,请回答有关问题:
| 族 周期 |
IA |
|
0 |
|||||
| 1 |
|
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
|
|
|
|
① |
|
② |
|
| 3 |
|
③ |
④ |
⑤ |
|
⑥ |
⑦ |
⑧ |
| 4 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)⑤和⑦的元素符号是__________和__________;
(2)表中最活泼的金属是__________,非金属最强的元素是__________(填写元素符号);
(3)表中能形成两性氢氧化物的元素是__________,分别写出该元素的氢氧化物与⑥和⑨的最高价氧化物的水化物反应的化学方程式:
__________________________________________________,
__________________________________________________,
(4)请设计一个实验方案,比较⑦和⑩单质氧化性的强弱:_____________________。
实验室常加热氯化铵与氢氧化钙固体制取氨气,写出该反应的化学方程式:,可用来检验氨气,现要制得2.24L(标况)氨气,理论上需要氯化铵固体g。(相对原子质量:N-14 H-1 Cl-35.5)
农村有句谚语“雷雨发庄稼”,这是由于在放电的条件下,空气中的氧气和氮气化合生成了氮的氧化物,氮的氧化物再经过各种复杂的化学变化,最后生成了易被农作物吸收的硝酸盐。
(1)写成有关反应的化学方程式
①
②
③
(2)以上哪个反应属于氮的固定?(填编号),请写出工业固氮的化学方程式
新制氯水呈色,说明氯水中有存在。向氯水中滴入几滴AgNO3溶液,立即有(填现象)生成,说明氯水中有存在,蓝色石蕊试纸遇到氯水后,会首先变红,但很快褪色,说明氯水具有性,氯水光照后,颜色,溶液的酸性,该反应的化学方程式是
己知A的分子结构模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等)。A~H有如下转化关系。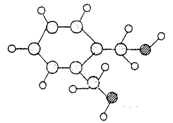

其中A、C、D的相对分子质量有如下关系:M(A)+M(D)= M(C);已知C能与碳酸钠反应放出二氧化碳。C和F、A和H在浓硫酸存在下共热,分别得到有机产物K和J,K和J分子中除苯环外,都含有一个8原子组成的环状结构。
(1)A的分子式为____________________.
(2)J的结构简式为________________________________________,
(3)K和J的关系满足(填序号)
A同类物质 B同分异构体 C同系物
(4)写出下列反应方程式:
反应②
反应④
(5)同时符合“①1mol该物质能和3mol NaOH反应②1mol该物质与足量的银氨溶液反应,生成4mol银单质”两项要求的C的同分异构体的数目为_______ 种,任写出其中的一种的结构简式。
.如图装置闭合电键K时,电流计A的指针将发生偏转。试回答:
(1) 丙池是(填“原电池”或“电解池”),甲中a极电极名称是,丙中c极电极名称是;
(2)乙中Cu极的电极反应是______,若电路中有0.02mol电子通过,则甲中a电极溶解的质量为g;
(3)闭合电键K一段时间后,丙池中生成二种气体和一种碱,则丙池中发生的总的化学方程式是;
(4)丙池中反应进行较长时间后,收集到标准状况下氢气2.24L此时测得丙池溶液质量实际减少4.23 g,含有碱0.100mol(不考虑气体在水中的溶解),则实际放出气体的物质的量是mol;
(5)如果要给丙中铁片上镀上一层Cu,则丙池应作何改进。