下图是温度和压强对X+Y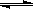 2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z反应影响的示意图。图中纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是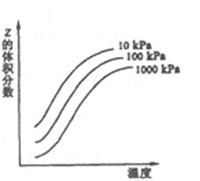
| A.X、Y、Z均为气态 |
| B.恒容时,混合气体的密度可作为此反应是否达到化学平衡[的判断依据 |
C.升高温度时 增大, 增大, 减小,平衡向右移动 减小,平衡向右移动 |
| D.使用催化剂Z的产率增加 |
中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是
| A.Na2O、Na2O2组成元素相同,推出与水反应产物也完全相同 |
| B.SO2和湿润的Cl2都有漂白性,推出二者混合后漂白性更强 |
| C.H2CO3的酸性比HClO强,推出CO2通入NaClO溶液中能生成HClO |
| D.根据常温下铜与浓硝酸反应可以制取NO2,推出常温下铁与浓硝酸反应也可以制取NO2 |
下列说法正确的是
A.将25℃纯水加热至95℃时, 增大 增大 |
B.将pH=11的Na2CO3溶液加水稀释, 增大 增大 |
| C.室温下,pH=a的盐酸与pH=b的氨水等体积混合后pH=7,则a+b="14" |
| D.0.1mol·L-酸HA与0.1mol·L-NaOH溶液等体积混合后pH>7,则 |

碘在地壳中主要以NaIO3的形式存在,在海水中主要以 的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法不正确的是
的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法不正确的是
| A.可用KI淀粉试纸和食醋检验加碘盐中是否含有碘 |
B.足量Cl2能使湿润的KI淀粉试纸变白的原因可能是 |
C.由图可知氧化性的强弱顺序为 |
D.途径Ⅱ中若生成1molI2,反应中转移的电子数为10 |
如图所示装置中,a、b都是惰性电极,通电一段时间后(电解液足量),a极附近溶液显红色。下列说法正确的是
| A.a是负极,b是正极 |
| B.CuSO4溶液的pH逐渐减小 |
C.铜电极上的反应式为 |
| D.向NaCl溶液中加入一定量的盐酸,能使溶液与原来溶液完全一样 |
某含碳、氢、氧的有机物A能发生如图所示的变化:已知A、C、D、E均能在一定条件下与新制的氢氧化铜悬浊液反应生成红色沉淀,则A的同分异构体是
| A.乙酸 | B.甲酸乙酯 | C.甲酸甲酯 | D.乙酸甲酯 |