一个原电池的总反应离子方程式是Zn + Cu2+ = Zn2+ + Cu,该反应的原电池组成正确( )
| |
A |
B |
C |
D |
| 正极 |
Zn |
Ag |
Cu |
Cu |
| 负极 |
Cu |
Cu |
Zn |
Zn |
| 电解质溶液 |
CuCl2 |
H2S04 |
CuSO4 |
FeCl2 |
下列图像能正确地表达可逆反应3A(g) + B(g) 2C(g)(△H<0)的是()
2C(g)(△H<0)的是()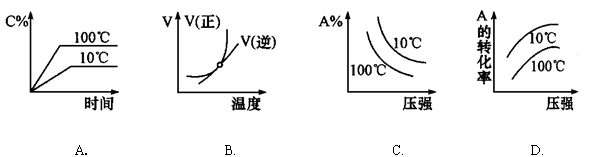
一定量的Fe和Fe2O3混合物投入2 mol·L-1 250 mL的HNO3溶液中,反应完全后,无固体剩余,生成1.12 L NO气体(标准状况),再向反应后溶液中加入1 mol·L-1的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是()
| A.450 mL | B.500 mL | C.400 mL | D.无法确定 |
现有一块已知质量的铝镁合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案
实验设计1:铝镁合金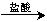 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积
实验设计2:铝镁合金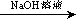 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积
实验设计3:铝镁合金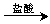 溶液
溶液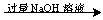 过滤,测定得到沉淀的质量
过滤,测定得到沉淀的质量
则能测定出镁的质量分数的是()
| A.都能 | B.都不能 | C.①不能,其它都能 | D.②③不能,①能 |
下列反应的离子方程式书写正确的是:()
| A.氯化铝溶液中加入过量氨水:Al3+ + 4NH3•H2O |
| B.NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3- + OH- +Ba2+ ="=" H2O + BaCO3↓ |
| C.碳酸氢铵溶液和足量氢氧化钠溶液反应: NH4+ + OH - =NH3·H2O |
D.NaAlO2溶液中通入少量CO2:2A1O2_+CO2+3H2O====2Al(OH)3↓+CO |
下列关于盐类的水解反应与中和反应的说法中,正确的是()。
| A.二者是同一反应 | B.两者没有任何联系 |
| C.盐类水解反应的逆反应是中和反应 | D.两者互为可逆反应 |