沼气是一种能源,它的主要成分是CH4。0.5 mol CH4完全燃烧生成CO2和液态水时放出445 kJ的热量,则下列热化学方程式中正确的是
| A.2CH4(g)+4O2(g)==2CO2(g)+4H2O(1)△H=" +1780" kJ/mol |
| B.CH4(g)+2O2(g)==CO2(g)+2H2O(l)△H=" +890" kJ/mol |
| C.CH4(g)+2O2(g)==CO2(g)+2H2O(1)△H= —890 kJ/mol |
D.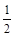 CH4(g)+O2(g)== CH4(g)+O2(g)==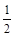 CO2(g)+H2O(1)△H= —890 kJ/mol CO2(g)+H2O(1)△H= —890 kJ/mol |
下列叙述正确的是
| A.Ca(OH)2的饱和溶液的导电能力很弱,所以Ca(OH)2是弱电解质 |
| B.CaCO3在水中溶解度虽然小,但溶解的CaCO3全部电离,所以CaCO3是强电解质 |
C.氨水和氯水的导电性很好 ,所以,一水合氨与氯气均为强电解质 ,所以,一水合氨与氯气均为强电解质 |
| D.SO2的水溶液能够导电,所以SO2属于电解质 |
下列有关Fe(OH)3胶体的制备方法正确的是
| A.将1~2ml饱和FeCl3溶液逐滴滴到20ml 0.5 mol·L-1NaOH溶液中 |
| B.将1~2ml饱和FeCl3溶液逐滴加入到20ml沸水中,并继续加热至溶液呈红褐色后停止加热 |
| C.将1~2ml饱和FeCl3溶液逐滴加入到20ml冷水中,再加热至沸腾 |
| D.将1~2ml沸水加入到1~2ml FeCl3饱和溶液中,并用玻璃棒不断搅拌 |
下列可以大量共存且溶液是无色的离子组是
| A.H+、Na+、NO3-、Cu2+ | B.Ba2+、Mg2+、Cl-、SO42- |
| C.H+、K+、OH-、NO3- | D.NO3-、SO42-、K+、Mg2+ |
设NA表示阿伏加德罗常数的数值,下列说法不正确的是
| A.16g氧气中所含的氧原子数为NA |
| B.18g水所含电子数为10NA |
| C.NA个氧气分子和NA个氢气分子的质量比为16∶1 |
| D.常温常压下,11.2LCl2含有的分子数为0.5NA |
在标准状况下,18gCO和CO2的混合气体的体积为11.2L。则此混合气体中CO和CO2的质量之比是
| A.1:1 | B.1:7 | C.1:11 | D. 7:11 7:11 |