A、B、C、D、E五种微粒,它们可能是原子或离子,并且所含的元素都在短周期。A显负价时,不能被任何氧化剂氧化;金属B的原子核内质子数比前一周期的同族元素多8,其单质不能从CuSO4溶液中置换出Cu;C元素有三种同位素,Cl、C2、C3,C1的质量数分别为C2、C3的1/2和1/3;D的气态氢化物溶于水后显碱性;E是由两种不同元素组成的带负电荷的微粒,它共有10个电子,E极易与C+结合成中性微粒。回答:
(1)写出五种微粒的符号:A 、B 、C 、D 、E 。
(2)C的同位素名称:C2 。
(3)C和D形成分子的电子式为 ,空间结构为 。
氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
(1)根据图1提供的信息,写出该反应的热化学方程式,
在图1中曲线(填“a” 或“b”)表示加入铁触媒的能量变化曲线。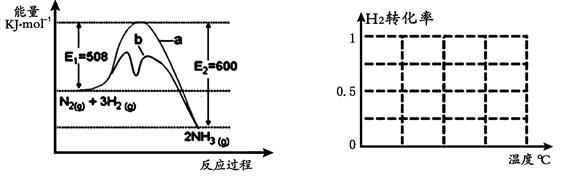
图1图2
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是
A.3v(H2)正=2v(NH3)逆 B.单位时间内生成nmolN2的同时生成2nmolNH3
C.混合气体的密度不再改变 D.容器内压强不随时间的变化而变化
(3)一定温度下,向2L密闭容器中充入1molN2和3molH2,保持体积不变,0.5min后达到平衡,测得容器中有0.4mol NH3,则平均反应速率v(N2)=,该温度下的平衡常数K=。若升高温度,K值变化(填“增大”、“减小”或“不变”)。
(4)为了寻找合成NH3的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
| 实验编号 |
T(℃) |
n (N2)/n(H2) |
P(MPa) |
| ⅰ |
450 |
1/3 |
1 |
| ⅱ |
_ |
_ |
10 |
| ⅲ |
480 |
_ |
10 |
A.请在上表空格中填入剩余的实验条件数据。
B.根据反应N2+3H2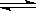 2NH3的特点,在给出的坐标图2中,画出其在1MPa和10MPa条件下H2的转化率随温度变化的趋势曲线示意图,并标明各条曲线的压强。
2NH3的特点,在给出的坐标图2中,画出其在1MPa和10MPa条件下H2的转化率随温度变化的趋势曲线示意图,并标明各条曲线的压强。
有机物A可以通过不同的反应得到下列物质:
B. C.
C. 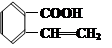
D.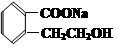 E.
E. 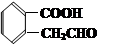
(1)A的结构简式是__________________
(2)写出由A制取B的化学方程式________________________
(3)写出A制取E这种物质的有机反应类型:______________; A与 __________(填写化学式)反应生成D。
(4)芳香族化合物F是A的同分异构体,1molF可以和3mol NaOH发生中和反应;F苯环上的一氯代物只有一种。写出F两种可能的结构简式 ______________________。
某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。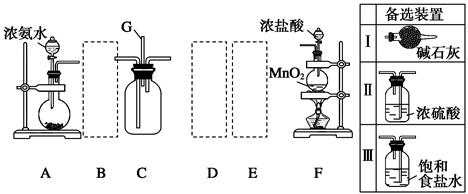
(1)装置F中发生反应的离子方程式:___________________。
(2)装置A中的烧瓶内固体可选用________(选填以下选项的代号)。
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择,并将编号填入下列空格:B__________,D__________,E__________。(均填编号)
(4)氯气和氨气在常温下相混就会反应生成氯化铵和氮气,装置C内出现浓厚的白烟并在容器内壁凝结,请设计实验方案鉴定该固体就是氯化铵:____________________________。
(5)从装置C的出气管口处逸出的尾气可能含有污染环境的气体,如何处理?________________________________________________________________________________。
(1)已知20oC时的溶解度:Na2CO3:S=21.2g; NaHCO3:S=9.6g。则20oC恒温条件下向121.2g饱和碳酸钠溶液中通入足量的CO2气体,理论上可以析出NaHCO3__________g(小数点后保留1位)
(2)向500mL KOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。若通入CO2气体为2.24L(标准状况下),得到11.9g的白色固体。则所用的KOH溶液的物质的量浓度为______mol/L。
(3)将一定质量的钠加入到89g水中,完全反应后的溶液为100g,则该溶液的质量分数为________。
(4)现有甲、乙两瓶无色溶液,已知它们可能是AlCl3溶液和NaOH溶液.现做如下实验:
①取440ml甲与120ml乙反应,产生1.56g沉淀;
②取440ml乙与120ml甲反应,也产生1.56g沉淀;
③取120ml甲溶液与400ml乙溶液反应,则产生3.12g沉淀;通过必要的计算和推理判定:
甲溶液为溶液,乙溶液为溶液。
(10分)已知A是治疗胃酸过多症的一种药剂,B是一种淡黄色固体,A、B以物质的量之比1∶1混合加热生成C、D、E三种物质,E、F、J是常见的气体单质,有如下转化关系: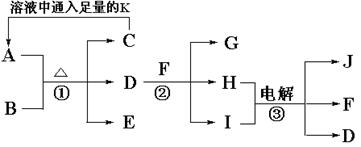
(1)写出A与D反应的离子方程式_________________________________________;
(2)写出反应②的化学方程式 __________________________________________。
(3)电解③时阳极产生气体168mL(标准状况),电解后溶液的体积为150mL,此时溶液的pH为________________。
(4)将等物质的量的A和C溶于100mL水中,下列溶液说法不正确的是_________。
A.2c(Na+)=3c(HCO3-)+3c(CO32-)+3c(H2CO3)
B.c(Na+)+ c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
C.c(CO32-)+2c(OH-)= 3c(H2CO3) + c(HCO3-) + 2c(H+)
D.c(Na+)> c(CO32-)> c(HCO3-)> c(OH-)> c(H+)
(5)若A、B混合后加热得到纯净物,反应的方程式为_________________________