在由铜片、锌片和200mL稀H2SO4组成的原电池中,若锌片只发生电化腐蚀。则当在铜片上共放出3.36 L(标准状况)的气体时,H2SO4恰好反应完。求:
(1)产生这些气体消耗的锌是多少g?
(2)有多少个电子通过导线?
(3)原稀硫酸的物质的量浓度是多少?
在由铜片、锌片和200 mL一定浓度的稀硫酸组成的原电池中,若锌片只发生电化学腐蚀,当在铜片上放出3.36 L(标准状况)的H2时,硫酸恰好用完,请填空并计算:
①正极的电极反应式为;负极的电极反应式为;
②通过导线的电子的物质的量;
③求原稀硫酸的物质的量浓度。
已知T℃、p kPa时,往容积可变的密闭容器中充入2 mol X和1 mol Y,此时容积为VL。保持恒温恒压,发生反应:2X(气)+Y(气)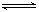 2Z(气),达到平衡时,平衡气中Z的体积分数为0.4。试回答下列有关问题:
2Z(气),达到平衡时,平衡气中Z的体积分数为0.4。试回答下列有关问题:
(1)使温度和压强在上述条件下恒定不变,再往上述密闭容器内充入4molZ,则反应达到平衡时,容器的容积为,平衡气中Z的体积分数为。
(2)若另选一个容积固定不变的密闭容器,仍控制温度为T℃,使3molX和1.5molY反应,达到平衡状态时,平衡气中Z的体积分数仍为0.4,则该密闭容器的容积为。
有机物A由碳、氢两种元素或碳、氢、氧三种元素组成。现取3g A与4.48L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重3.6g,碱石灰增重4.4g。回答下列问题:
(1)3gA中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
由铜片、锌片和200mL稀硫酸组成的原电池中,当铜片上放出3.36L(标状况)气体时(锌片上无气体产生),硫酸恰好反应完.计算:
(1)产生这些气体消耗的金属是哪一种,消耗的质量是多少;
(2)有多少电子通过了导线;
(3)硫酸溶液的物质的量浓度是多少.
将Cu与CuO的混合物20.8g加入到50mL 18.4mol/L浓H2SO4中,加热充分反应至固体物质完全溶解,冷却后将混合液稀释至1000 mL,测得c(Cu2+ )="0.3" mol/L。试计算:(本题无计算过程不给分)
)="0.3" mol/L。试计算:(本题无计算过程不给分)
(1)反应过程中放出的 气体在标准状况下的体积(不考虑气体在溶液中的溶解)。
气体在标准状况下的体积(不考虑气体在溶液中的溶解)。
(2)溶液稀释后,c(H+)是多少?