化学中质量守恒定律是一个非常重要的定量定律。
(1)如下图装置中,称量小烧杯中所有物质的质量m1,然后将小烧杯中的碳酸钠与盐酸完全混合,反应发生一段时间后,再称量小烧杯及烧瓶内物质的总质量为 m2,则(填“=” “>”“<”)m1 m2,其原因为 。 
(2)天然气的主要成分是甲烷(CH4),可直接用作气体燃料。燃烧反应前后分子种类变化的微观示意图如下所示。
①1个B分子中含有 个原子。
②四种物质中属于化合物的是 (填图中字母)。
(3)A和B可发生如下反应:3A+2B=A3B2,某学生做了3次该实验(每次均充分反应),反应前A和B的质量 和都是l0g。有关实验数据见下表:
序号 反应前A的质量 反应前B的质量 反应后A3B2的质量
① 8g 2g 6g
② 4g 6g 6g
③ xg yg 9g
X∶Y的比值可能为 或 。
(4)为了测定某品牌食用纯碱中碳酸钠的质量分数,某校化学研究性学习小组的探究过程如下:
《提出问题》样品中碳酸钠的质量分数是多少?
《知识准备》食用纯碱的主要成分是碳酸钠,另外还含有少量的氯化钠;反应过程中不考虑水和氯化氢的挥发。
《设计方案》(1)方案一:向一定量样品中加入过量澄清石灰水,根据反应生成碳酸钙的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数。
(2)方案二:向一定量样品中加入足量的稀盐酸,根据反应生成二氧化碳的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数。
《进行实验》甲组同学:称取24.00g样品,加水配成溶液,在溶液中加入过量的澄清石灰水。过滤、洗涤、干燥,共得到白色沉淀20.00g。
乙组同学:称取24.00g样品,加入足量的稀盐酸直到反应停止,共收集到8.80g二氧化碳。
《解决问题》请你任选一组同学的实验结果,帮助他们计算出样品中碳酸钠的质量分数。(写出计算过程。计算结果精确到0.1% )
在金属活动性顺序里,钠位于铜之前。某化学兴趣小组发现,将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,却未置换出红色的铜。该小组同学对此现象进行了如下探究:
【查阅资料】钠的化学性质非常活泼,常温下就能被空气中的氧气氧化,且能与水迅速反应。
【分析与讨论】
(1)在实验室中通常将钠保存在煤油里,煤油的作用是。
(2)已知:在一个化学反应中,如果有元素化合价的升高,同时就有元素化合价降低。对于钠与水反应的生成物,甲同学猜想是NaOH和H2,乙同学猜想是NaOH和O2,你认为同学的猜想不合理,请从化合价的角度解释原因:。
【进行实验】该小组同学通过实验验证钠与水反应的产物,装置如下图: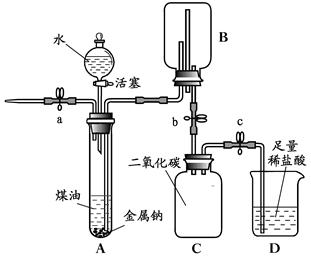
注:煤油的密度为0.8g/mL,与水不互溶。
| 实验操作 |
实验现象及分析 |
|
| ① |
打开止水夹a及分液漏斗活塞,待液体充满大试管后,关闭止水夹a及分液漏斗活塞。 |
实验现象为:液体分层,钠熔成银白色小球,在液体分层的界面上跳动,产生大量气泡,下层液体逐渐被压入B中。 钠的物理性质有:(任写两条)。 |
| ② |
打开止水夹b,待B中部分液体进入C中,迅速关闭止水夹b。 |
发生反应的化学方程式为: 。 |
| ③ |
打开止水夹c。 |
实验现象为:D中液体,C中产生气泡。 |
| ④ |
打开止水夹a,通过分液漏斗向大试管中逐滴加水,将燃着的木条伸至装置左端尖嘴导管口。 |
实验现象为:气体燃烧,产生色火焰。 |
| ⑤ |
在火焰上方罩一个干冷的烧杯。 |
实验现象为:烧杯内壁出现。 |
【解释与结论】将钠投入硫酸铜溶液中,产生无色气体和蓝色沉淀,写出发生反应的化学方程式(分两步写):,。
根据下列装置图,回答有关问题:
(1)写出装置中标号仪器的名称:a,b。
(2)实验室制取氧气时选用A作为发生装置,若试管中是混有二氧化锰的氯酸钾,该反应的化学方程式为;若试管中是高锰酸钾,则需要在试管口放一团棉花,其目的是。
(3)实验室制取二氧化碳时选用B作为发生装置,该反应的化学方程式为;选用C作为收集装置,则检验二氧化碳是否已收集满的方法是。
(4)实验室用锌粒与稀硫酸反应制取氢气,发生装置如右图所示。打开止水夹,若发现稀硫酸未能与有孔塑料板上的锌粒接触,但此时已无稀硫酸可加,则下列溶液中,最适宜从长颈漏斗中添加的是(选填字母)。
| A.氢氧化钠溶液 | B.碳酸钠溶液 |
| C.硫酸钠溶液 | D.澄清石灰水 |
某化学兴趣小组对CO2是否支持常见金属的燃烧进行探究活动。
【活动一】探究CO2是否支持实验室常见金属镁的燃烧
实验①:将镁条用细砂纸打磨光亮,在酒精灯上点燃,再将燃着的镁条插入充满CO2的集气瓶,发现镁条仍燃烧。生成物除白色MgO外,还有一种黑色固体。
⑴、将镁条用细砂纸打磨光亮,是为了。
⑵、镁在CO2中反应的化学方程式为,此反应的基本类型是。
⑶、实验①的结论是。由该结论可知(写“能”或“不能”)用CO2灭火器扑灭活泼金属的火灾。
⑷、通过实验①你对燃烧条件的新认识是。
【活动二】探究CO2是否支持生活中常见金属铁的燃烧,兴趣小组设计如下方案:(本题回答正确将奖励4分,但化学试卷总分不超过60分。)
方案①:将弯成螺旋状的细铁丝系上一支火柴,点燃火柴,待火柴快燃尽时,插入装有CO2的集气瓶中,观察铁丝能否被引燃。
方案②:将弯成螺旋状的细铁丝系上一段镁带,点燃镁带,待镁带快燃尽时,插入装有CO2的集气瓶中,观察铁丝能否被引燃。
实验评价:你认为方案(填①或②)更为科学。
理由是:
。
下列装置常用于实验室制取气体。根据给出的装置回答下列问题:
(1)指出编号仪器名称:①,②。
(2)利用C装置收集氧气的最佳时刻是。
用收集到的氧气完成硫粉燃烧实验后,还需向集气瓶内加入适量氢氧化钠溶液,目的是:(用化学方程式表示)。
(3)制取并收集二氧化碳应选择的装置是(从A——E中选择),若改用F装置收集二氧化碳,则气体应从端进入。
(4)将纯净的二氧化碳气体通入盛有蒸馏水的洗气瓶一段时间后,测得该装置中溶液的pH(填“>”、“<”或“=”)7。
小刚在化学实验室发现,盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末。小刚叫来小军和小红,共同探究这种白色粉末的成分。他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:
【提出猜想】①可能是NaOH;② 可能是Na2CO3; ③ 可能是。
【实验探究】他们分别做了下面的实验。
(1)小军取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色。由此小军认为白色粉末是NaOH。请判断小刚所得结论是否正确,_______(填“正确”或“不正确”),并简述理由:
____________________________________________________________________。
(2)小红取少量白色粉末溶于水,向所得溶液中滴加BaCl2试液,有白色沉淀产生。由此判断白色粉末中含有______。为了验证猜想③,小红继续向溶液中滴加BaCl2试液至不再产生沉淀,然后过滤。你认为她接下来还应进行的实验是 。
【实验反思】在小红所做的实验中,若把BaCl2溶液换成Ba(OH)2溶液是否可行?________(填“是”或“否”),请简述理由。_______________________________________________________。