具有相同电子层数,原子序数相连的三种短周期元素X、Y、Z,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4,则下列判断正确的是
| A.气态氢化物的稳定性:HX<H2Y<ZH3 | B.非金属活泼性:Y<X<Z |
| C.原子半径:X>Y>Z | D.原子最外层上的电子数关系:Y=" (X+Z)/2" |
有一无色透明的溶液,要确定是否含有以下离子:H+、K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下:
| 实验步骤 |
实验现象 |
| (1)取少量该溶液,加几滴紫色石蕊溶液 |
溶液变红色 |
| (2)取少量该溶液加热浓缩,加Cu片和浓H2SO4,加热 |
有无色气体产生,气体遇空气可以变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 |
有白色沉淀生成 |
| (4)取(3)中上层清液,加AgNO3溶液 |
有稳定的白色沉淀生成,且不溶于HNO3 |
| (5)取少量该溶液,加NaOH溶液 |
有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
由此判断:
(1)溶液中肯定存在的离子是,溶液中肯定不存在的离子是。
(2)为进一步确定其他离子,应该补充的实验及对应欲检离子的名称(如为溶液反应,说明使用试剂的名称,不必写详细操作步骤)。。
(1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气,写出该反应的离子方程式;
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。 漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为;
(3)在下图的四条直线分别表示钠、铜、铝、铁与足量Cl2反应时,消耗金属的质量(纵轴)与反应掉的氯气质量(横轴)的关系,其中代表铁与Cl2反应的直线是,如果横轴表示消耗掉的硫的质量,则b表示的是四种金属中的。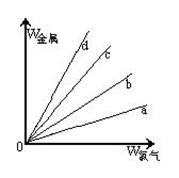
常温下,一种烷烃A和一种单烯烃B组成的混合气体,A或B分子最多只含有4个碳原子,且B分子的碳原子数比A分子的多。
(1)将1L混合气体充分燃烧,在同温同压下得到2.5LCO2气体。试通过计算推断原混合气体中A和B所有可能的组合及其体积比,并将结果填入下表:
| 组合编号 |
A的分子式 |
B的分子式 |
A和B的体积比(VA :VB) |
| ① |
|||
| ② |
|||
| ③ |
|||
| ④ |
为进一步确定A、B分子式,继续实验:
(2)120℃时,取1L该混合气体与9L氧气混合,充分燃烧后,当恢复到120℃和燃烧前的压强时,体积增大了6.25﹪。试通过计算确定唯一符合题意的A、B的分子式。
有机化学反应因反应条件不同,可生成不同的有机产品。例如:
(1)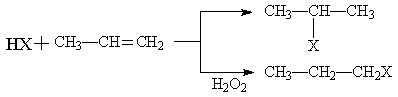 (X为卤素原子)
(X为卤素原子)
(2)苯的同系物与卤素单质混合,若在光照条件下,侧链上氢原子被卤素原子取代;若在催化剂作用下,苯环上的氢原子被卤素原子取代。
(3)R—CH2OH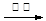 RCHO,
RCHO,
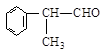 工业上利用上述信息,按下列路线合成结构简式为的物质,该物质是一种香料。
工业上利用上述信息,按下列路线合成结构简式为的物质,该物质是一种香料。
请根据上述路线,回答下列问题:
(1)A的结构简式可能为、。
(2)反应①、③、⑤的反应类型分别为、、。
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件):。
(4)工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法,其原因是。
在催化剂和加热条件下,环丁烷和氢气能发生反应: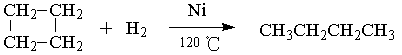
碳原子数不大于4的环烷烃可与卤素发生上述类似反应,而碳原子数大于4的环烷烃与卤素则发生取代反应。根据以上信息,完成下列问题:
一定条件下,由环丁烷可得到1,3—丁二烯(CH2=CH—CH=CH2),请用化学反应方程式表示出最简单的制备方案:。