现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示。
| 硫酸(500mL) 品名:硫酸 化学式: 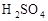 密度: 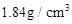 质量分数:98% 质量分数:98% |
(1)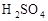 的相对分子质量是 。
的相对分子质量是 。
(2)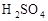 分子中,H、S、O的原子个数比为 。
分子中,H、S、O的原子个数比为 。
(3)该瓶浓硫酸的质量为 g。
(4)用100g98%的该浓硫酸稀释成19.6%的稀硫酸,需要水多少g?
(5)某同学用锌粒与19.6%的稀硫酸反应制取氢气,反应所用的稀硫酸和生成氢气的关系如右图。
计算:
①至少需要多少g的锌粒?
②完全反应后所得溶液的溶质质量分数为多少?
(保留一位小数点)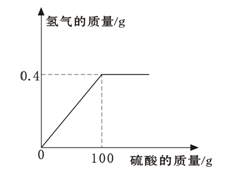
国家质量规定,市场出售尿素[CO(NH2)2]的含量在96%以上的为一级品,供销社出售一批尿素,其含氮量为45% ,通过计算这批尿素可否按一级品出售?
葡萄糖(化学式为C6H12O6)是一种有甜味、易溶于水的白色粉末状固体。葡萄糖在人体内发生缓慢氧化转化为二氧化碳和水,并释放出热量。下面是有关葡萄糖的一些计算。
(1)葡萄糖中各元素的最简质量比为C:H:O= ;
(2)葡萄糖中各元素的原子个数比为C:H:O= ;
(3)葡萄糖中氢元素的质量分数为 (保留一位小数)
在2010年春季,安徽阜阳地区发生了震惊全国的“毒奶粉”事件。劣质奶粉制造商为牟取暴利,大大降低了奶粉中蛋白质的含量,导致食用这种奶粉的众多婴儿严重营养不良乃至死亡。奶粉中蛋白质含量的国家标准为:每100克婴儿奶粉中含12—15克蛋白质。其测定方法是:奶粉经系列反应生成氨,由氨计算出氮元素的质量,再由氮求出蛋白质的质量(蛋白质含氮按16%计算)。今有一袋从农村市场查获的奶粉,取样品100克,反应后生成的氨气和7.5克19.6%的稀硫酸恰好完全反应〔2NH3+H2SO4====(NH4)2SO4〕,试通过计算判断这袋奶粉是否属于劣质奶粉。
市售某种氮肥中,主要成分为尿素[化学式为:CO(NH2)2]若含量在96%以上为达标一级产品。请回答:
⑴尿素的相对分子质量是;其中氢和氧元素质量比为 _____________,氮元素的质量分数为_________。(保留一位小数)
⑵经测定该化肥的氮元素质量分数为45%,请计算确定是否达到一级品标准。
⑶某农民向田里使用50千克的这种化肥,如果改用NH4NO3 需要购买多少千克才能有相同量的氮元素(保留一位小数)
黄梅马鞍山出产铁矿石,经化学分析,铁矿石的主要成分为氧化铁,其中含泥沙等杂质,求:
(1)氧化铁的相对分子质量为。
(2)纯氧化铁中铁元素质量分数为。