(6分)在化学实验技能考试做完“二氧化碳的制取和性质”实验后,废液桶中有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质)。为避免污染环境并回收利用废液,化学兴趣小组做了如下实验:
取废液桶上层清液共11.88kg,向其中加入溶质质量分数为21.2%的碳酸钠溶液。所得溶液pH与加入的碳酸钠溶液的质量关系如右图所示:
(1)通过右图可知,当碳酸钠溶液质量加到 kg时,废液恰好处理完(盐酸与氯化钙的混合溶液完全转化成氯化钠溶液)。
(2)此时所得溶液能否用于该校生物兴趣小组的小麦选种(选种液要求氯化钠的溶质质量分数在10%~20%之间)?请通过计算回答。
随机抽取市售某种“纯碱”样品,经检验杂质仅是氯化钠。准确称取样品20克,加入100克稀盐酸溶液使其恰好完全反应,将反应后的剩余物质称量,质量为117.8克。
(1)生成二氧化碳质量是克。
(2)所用稀盐酸的质量分数是多少?
为研究某含C、H、O元素的有机物的组成,将8.00g该有机物在氧气中充分燃烧,并将生成物全部通过如图的装置,测得下表的结果。(提示:氯化钙是干燥剂)

求:①该有机物所含各元素的质量;
②该有机物中C元素的质量分数;
③该有机物的化学式(最简式)。
某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5 g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收。测得吸收氨气的溶液总质量m与反应时间t的变化如下图所示。所涉及的反应为: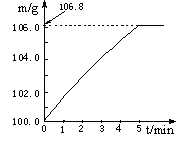
(NH4)2SO4+2NaOH Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4=(NH4)2SO4。
Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4=(NH4)2SO4。
请计算:
(1)完全反应后产生氨气g。
(2)该化肥的含氮量为 (精确到0.1%),则这种化肥属于(填:“合格”或“不合格”。合格硫酸铵含氮量为20%以上)产品。
(3)请计算废硫酸中硫酸的质量分数(写出计算过程)。
(4)若实验过程中氨气被完全吸收,但该实验测得硫酸铵化肥的含氮量高于实际值,其原因是。
为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出)。产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算:
⑴A点产生气体的质量为;
⑵试样中碳酸钠的质量分数(结果精确到0.1%);
⑶B点时,烧杯内溶液中溶质的化学式。
为从定量角度认识中和反应,小明同学自行设计并进行了下面实验:
①在小烧杯中倒入8%的氢氧化钠溶液l0g,滴入2滴酚酞试剂后,溶液呈红色;
②另取10%的稀盐酸逐滴滴加到氢氧化钠溶液中,边滴边振荡,随盐酸滴入,溶液颜色逐渐变浅;
③在溶液红色消失瞬间,停止实验。
若停止实验时,两溶液恰好反应。请分析小明实验后回答:
(1)实验中酚酞试剂的作用是__________________________;
(2)计算出这时共用去稀盐酸的质量是多少?(精确到0.1)