某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量的关系如图所示。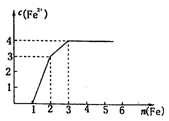
溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为
| A.1:1:1 | B.1:3:1 | C.1:1:4 | D.3:3:8 |
某工厂排放的工业废水中可能含有K+、H+、Mg2+、SO42-、Cl-、NO3-等离子。经检测废水呈明显的碱性,则可确定该厂废水中肯定不含有的离子组合是( )
| A.H+、Mg2+ | B.K+、NO3-、SO42- |
| C.H+、K+、NO3- | D.K+、Mg2+、SO42-、Cl- |
硅单质及其化合物在材料领域中一直扮演着主要角色。下列叙述中,不正确的是( )
| A.石英可用来制作工艺品 |
| B.硅单质可用来制造太阳能电池 |
| C.硅单质是制造玻璃的主要原料 |
| D.二氧化硅是制造光导纤维的材料 |
下列应用或事实与胶体的性质没有关系的是( )
| A.在河流入海口处易形成三角州 |
| B.用石膏或盐卤点制豆腐 |
| C.尿毒症患者做“血液透析” |
| D.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀 |
下列物质分类正确的是( )
| A.Cu(OH)2难溶于水,属于非电解质 |
| B.NH4Cl组成中不含金属离子,不属于盐 |
| C.SO2溶于水能导电,SO2属于电解质 |
| D.HCl气体溶于水电离成H+和Cl-,属于电解质 |
30 mL 1 mol/L NaCl溶液和40 mL 0.5 mol/L CaCl2溶液混合之后(体积的变化忽略不计),混合液中Cl-的物质的量浓度为( )
| A.0.5 mol/L | B.0.6 mol/L | C.1 mol/L | D.2 mol/L |