某研究性学习小组设计不同实验方案来研究硝酸的性质。
(1)甲组同学设计下图装置来证实稀硝酸与铜反应,步骤如下。
A、检验50ml针筒的气密性。
B、抽出活栓,往针筒内放入一小块铜片,把针筒活栓推到底,将针筒下端玻璃管浸入蒸馏水中,抽拉活栓,吸入约10mL蒸馏水,发现针筒内仍有空气,然后 。
C、将针筒下端玻璃管浸入浓硝酸中,抽拉活栓,缓缓吸入4mL浓硝酸,将针筒下端套上橡皮管,然后用铁夹夹住。
回答以下相关问题:
①B中应补充的操作是 。
②一段时间后在针筒内观察到溶液颜色为蓝色,有 色气体产生。该反应的离子方程式为 。
③反应停止后,针筒内产生了气体,要验证产生的气体是NO,还需进一步进行的操作是 。
(2)乙组同学也用此装置直接抽取浓硝酸和铜反应,发现溶液是绿色的,为了探究绿色的原因,乙组同学又做了三组对比实验,具体如下:
| 组 |
m(Cu)/g |
硝酸(过量) |
溶液颜色 |
| A |
1 |
浓HNO3(4mL) |
溶液为绿色 |
| 1 |
稀HNO3(4mL) |
溶液为蓝色 |
|
| B |
0.5 |
浓HNO3(4mL) |
溶液为绿色 |
| 1 |
稀HNO3(4mL) |
溶液为蓝色 |
|
| C |
2 |
浓HNO3(4mL) |
溶液为绿色 |
| 1 |
稀HNO3(4mL) |
溶液为蓝色 |
根据乙组同学三组对比实验回答问题:
①一种观点认为:这可能是Cu2+浓度差异的结果,你同意这种看法吗?(填“同意”或“不同意”)__________,原因是 。(结合表格信息加以阐述)
②另一种观点认为:溶液呈绿色是铜与浓硝酸反应时产生的NO2溶于过量浓硝酸显黄色,加上和蓝色的硝酸铜溶液混在一起,使溶液呈绿色。为了验证推断是否正确,三位同学分别设计了三种方案,并进行验证:
方案一:将绿色溶液转移至试管,并给试管加热片刻,立即看到大量红棕色气体产生。认为该气体一定是溶解在溶液中的NO2,但也有同学持有异议。请分析原因 。
方案二:用双氧水和二氧化锰制得氧气,并把氧气缓缓通入绿色溶液中,观察溶液颜色变为蓝色。请用方程式表示溶液颜色变化的反应原理__________ ____________。
方案三:往蓝色溶液中缓缓通入NO2气体,溶液颜色变绿色。
③从环保的角度看,你认为三个方案中最好的是哪一个 。
CH3Cl为无色,略带臭味的气体,密度为2.25g/L,熔点为-24.2℃,易溶于乙醇和丙醇等有机溶剂。
Ⅰ.实验室制取CH3Cl的原理是CH3OH+HCl(浓) CH3Cl+H2O.具体步骤如下:
CH3Cl+H2O.具体步骤如下: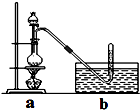
①干燥ZnCl2晶体;
②称取24g研细的无水ZnCl2和量取20mL浓盐酸放入圆底烧瓶,同时量取一定量的甲醇放入分液漏斗中
③将分液漏斗里的甲醇逐滴滴入烧瓶中并加热,待ZnCl2完全溶解后有CH3Cl气体逸出,可用排水法收集
请回答:
(1)实验室干燥ZnCl2晶体制得无水ZnCl2的方法是________________;
(2)反应过程中滴入烧瓶中甲醇的体积比盐酸少(甲醇与浓盐酸的物质的量浓度接近)其理由是__________;
(3)实验室为何用排水法收集CH3Cl?________________;
Ⅱ.据某资料记载,CH4分子中的一个H原子被Cl原子取代后,其稳定性受到影响,可被强氧化剂酸性高锰酸钾氧化,现有四只洗气瓶:分别盛有以下试剂:
| A.1.5%KMnO4(H+)溶液; | B.蒸馏水; | C.5%Na2SO3溶液; | D.98%H2SO4. |
(1)为证实这一理论的可靠性,请从上面选择最恰当的洗气瓶,将a装置生成的气体依次通过洗气瓶__________(填洗气瓶编号),如果观察到_____________则证实上述资料的正确性。
(2)写出洗气瓶中发生反应的离子方程式(C元素的氧化产物为CO2):________________;
(3)如果CH3Cl是大气的污染物,上述洗气瓶之后还应接一只盛__________的洗气瓶。
某天然碱样品的组成可能为aNa2CO3·bNaHCO3·cH2O(a、b、c为正整数)。为确定其组成,某小组进行如下实验:
(1)定性实验
①取少量天然碱样品放入试管中,用酒精灯加热,在试管口有液体生成,该液体能使无水硫酸铜变蓝.能否说明样品中含结晶水,试简述理由________________;
②请设计一个简单方案,确认样品中含有CO32-____________________。
(2)定量分析
该同学设计了如图所示装置,测定天然碱的化学组成.
实验步骤:
①组装好实验装置后,首先进行的操作是___________;A处碱石灰的作用是:__________;E处碱石灰的作用是__________________。
②称7.3g样品,放入硬质玻璃管中;称量C装置质量为87.6g,D装置为74.7g。
③打开活塞K1、K2,关闭K3,通人空气数分钟。
④关闭活塞Kl、K2,打开K3,点燃酒精灯至不再产生气体为止。
⑤打开活塞Kl,鼓人空气数分钟,然后称得C装置质量为88.5g;D装置质量为75.8g,通入空气的目的是____________________。
⑥该天然碱的化学式为_______________。
(I)pH的测定是中学化学中重要的定量实验。
(1)下列关于pH测定的说法正确的是 。
a.用pH试纸测得某盐酸的pH=2. 3
b.将pH试纸直接插入待测溶液,取出后再与标准比色卡对比
c.用pH试纸测新制氯水的pH
d.能使pH试纸显红色的溶液显酸性
(2)某同学先用蒸馏水润湿pH试纸,再用该试纸分别测定c(OH-)相等的NaOH溶液和氨水的pH,误差较大的是 。
(II)常温下,甲、乙、丙三位同学用实验确定某酸HA是弱电解质的方案分别是:
甲:用pH试纸测定0.1 moI/L HA溶液的pH,即可证明HA是弱电解质。
乙:①分别取pH=l的HA溶液和稀盐酸各10.00 mL,再加水稀释为100 mL。
②各取相同体积的两种稀释液(适量),同时分别加入纯度和形状大小均相同的锌粒(足量),观察现象,即可证明HA是弱电解质。
丙:将适量的HA溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,分析表中数据可以说明HA是弱电解质。
| 编号 |
NaOH/mol·L-1 |
HA/mol·L-1 |
混合溶液的pH |
| ① |
0.1 |
0.1 |
pH=9 |
| ② |
c |
0.2 |
pH=7 |
| ③ |
0.1 |
0.2 |
pH<7 |
(1)甲的方案中,说明HA是弱电解质的理由是测得溶液的pH_______1(填“>”、“<”或“=”)。
(2)在乙的方案的第①步中,需要用到的定量仪器是 。
(3)乙的方案中,说明HA是弱电解质的主要现象是_________(填字母)。
A.装稀盐酸的试管中放出H2的速率快
B.装HA溶液的试管中放出H2的速率快
C.两个试管中产生气体的速率一样快
(4)丙的方案中,编号②中的c_______(填“>”、“<”或“=”)0.l。
(5)丙的方案中,编号③的数据表明,混合溶液中HA的电离程度比NaA的水解程度:________(填“强”、“弱”或“无法确定”)。
某学生为了探究钠与CO2的反应,利用如图装置进行实验.(已知PdCl2能被CO还原得到黑色的Pd)
(1)请将上图各装置连接完整(填写装置中字母):c接f, 接 , 接 ,接 。
(2)若用稀盐酸与CaCO3反应制备CO2,在加稀盐酸时,发现CaCO3与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是 。
| A.NaNO3溶液 | B.CCl4 | C.苯 | D.稀硝酸 |
(3)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让CO2充满整个装置,当观察到 时再点燃酒精灯。
(4)反应过程中CO2足量,假如反应过程中有下列两种情况,分别写出两种情况下钠与CO2反应的化学方程式 。
Ⅰ.装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体 。
Ⅱ.装置①中钠的质量为0.46g,充分反应后,将装置①中的固体加入到足量稀盐酸中产生224mL(标准状况)CO2气体,且溶液中还有固体残留 。
某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是________;
(2)实验过程中,装置B中发生的现象是________,这个现象分别说明SO2具有的性质是________;
(3)装置C中Na2S溶液在空气中不易保存,时间长了会变浑浊,原因是(用离子方程式表示)____;
(4)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象_________________;
(5)如果把分液漏斗中的浓硫酸换成浓HNO3,对此实验是否有影响________(填“是”或“否”)。请说明你的理由___________________;
(6)工业上用黄铜矿(CuFeS2)冶炼铜,副产品中也有SO2,冶炼铜的反应为:8CuFeSO2+2IO2 8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中 Fe 的化合价为+2,反应中被还原的元素是________(填元素符号),当生成0.8mol铜时,此反应转移的电子数目是________。
8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中 Fe 的化合价为+2,反应中被还原的元素是________(填元素符号),当生成0.8mol铜时,此反应转移的电子数目是________。