某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是________;
(2)实验过程中,装置B中发生的现象是________,这个现象分别说明SO2具有的性质是________;
(3)装置C中Na2S溶液在空气中不易保存,时间长了会变浑浊,原因是(用离子方程式表示)____;
(4)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象_________________;
(5)如果把分液漏斗中的浓硫酸换成浓HNO3,对此实验是否有影响________(填“是”或“否”)。请说明你的理由___________________;
(6)工业上用黄铜矿(CuFeS2)冶炼铜,副产品中也有SO2,冶炼铜的反应为:8CuFeSO2+2IO2 8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中 Fe 的化合价为+2,反应中被还原的元素是________(填元素符号),当生成0.8mol铜时,此反应转移的电子数目是________。
8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中 Fe 的化合价为+2,反应中被还原的元素是________(填元素符号),当生成0.8mol铜时,此反应转移的电子数目是________。
物质的加热是中学化学实验的重要基本操作。常用加热方式有3类:①直接在酒精灯上加热;②通过石棉网用酒精灯加热;③通过水浴加热。以下10个中学化学实验中有的要加热,有的不要加热:
| A.用双氧水和二氧化锰制取氧气 | B.食盐溶液蒸发制取氯化钠晶体 |
| C.氯化铵与碱石灰反应制取氨气 | D.浓硝酸和铜反应制取二氧化氮气体 |
E.乙醇和浓硫酸制取乙烯 F.石油的分馏
G.苯与溴在铁催化下制取溴苯 H.乙醛溶液与银氨溶液发生银镜反应
I.乙酸乙酯在酸性条件下发生水解 J.葡萄糖与新制的氢氧化铜悬浊液反应
其中:
(1)可用酒精灯直接加热的有(填写字母代号,多选倒扣分,下同)。
(2)用酒精灯通过石棉网加热的有。
(3)通常用水浴加热的有。
第29届奥运会祥云火炬的外壳材料是高强度的铝镁合金。某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数,他们利用盐酸、氢氧化钠溶液设计了三种不同的实验方案:
方案一:铝镁合金 测定生成气体的体积
测定生成气体的体积
方案二:铝镁合金 测定生成气体的体积
测定生成气体的体积
方案三:铝镁合金 溶液
溶液
 称量灼烧产物的质量。
称量灼烧产物的质量。
(1)实验小组根据方案二设计了两个实验装置,如下圈(图中的铁架台已省略)。
你认为选择(选填甲或乙)装置进行实验更合理,误差更小。
(2)用方案三进行实验时,除了称量灼烧产物质量外,还需称量的是。
(3)拓展研究:在向铝镁合金溶于盐酸后的溶液中加入过量 溶液时,生成沉淀的质量与加入
溶液时,生成沉淀的质量与加入 溶液体积的关系可用数轴关系表示:
溶液体积的关系可用数轴关系表示:
请你判断,根据上图数轴申的数据能否求出合金中镁的质量分数? (选填“能”或“不能”)
下列①②两题选一题作答。
①若不能求出合金中镁的质量分数,请说明理由。
②若能求出合金中镁的质量分数,则镁的质量分数为。
氯气是一种重要的化工原料,在生产和生活中应用十分广泛。
已知: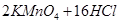 (浓)="==="
(浓)="===" 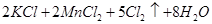 ,
,
在实验室可用二氧化锰固体或高锰酸钾固体和浓盐酸反应制取氯气。可供选用的发生装置如下图。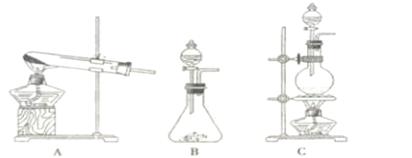
(1)若用高锰酸钾固体和浓盐酸反应制取氯气,发生装置是。(选填A或B或c)
(2)写出用二氧化锰固体和浓盐酸反应制取氯气的化学方程式:。
(3)实验室收集氯气的方法是。
(4)常用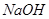 溶液吸收氯气防止污染。写出该反应的离子方程式。
溶液吸收氯气防止污染。写出该反应的离子方程式。
实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案: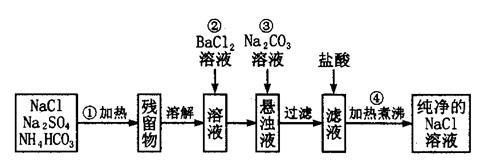
如果此方案正确,那么:
(1)操作①可选择_____或_____仪器。
(2)操作②是否可改为加硝酸钡溶液?为什么?_______________________________。
(3)进行操作②后,如何判断SO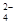 已除尽,方法是__________。
已除尽,方法是__________。
(4)操作③的目的是_________,为什么不先过滤后加碳酸钠溶液?理由是________。
(5)操作④的目的是____________________________________。
⑴实验操作中,不慎将手指划破,这时可从急救箱中取FeCl3溶液止血,其原理是。
⑵今有两瓶标签模糊不清,只知道分别盛有淀粉溶液和氯化钠溶液,试用多种方法对其鉴别。
①。
②。