短周期元素X、Y的原子序数相差2。下列有关叙述不正确的是( )
| A.X与Y可能位于同一主族 |
| B.X与Y不一定位于同一周期 |
| C.X与Y可能形成离子化合物XY |
| D.X与Y不可能形成共价化合物XY |
右图是298K 时N2与H2反应过程中能量变化的曲线图。下列叙述不正确的是
A.该反应的热化学方程式为:N2(g) + 3H2(g)  2NH3(g) ΔH = -92kJ·mol-1 2NH3(g) ΔH = -92kJ·mol-1 |
| B.b曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂, 该化学反应的活化能和反应热都改变 |
| D.在温度体积一定的条件下, 通入lmol N2和3molH2反应后放出的热量为Q1kJ, 若通入2molN2和6molH2反应后放出的热量为Q2kJ 则184>Q2 >2Q1 |
铅蓄电池的电极材料是Pb和PbO2,电解液是硫酸溶液。现用铅蓄电池电解饱和硫酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法不正确的是
| A.蓄电池放电时,每消耗0.1molPb,共生成0.1molPbSO4 |
| B.电解池的阳极反应式为:4OH-- 4e-==2H2O + O2↑ |
| C.电解后,c(Na2SO4)不变,且溶液中有晶体析出 |
| D.蓄电池中每生成2molH2O,电解池中就消耗1molH2O |
下列与化学反应能量变化相关的叙述正确的是
| A.生成物总能量一定低于反应物总能量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g) |
已知有如下平衡体系:3A(g) + B(g) 2C(g),现等物质的量的投料反应物A、B于恒温恒容体系I和恒温、恒压体系II中,达平衡时体系I中A的物质的量浓度为M,体系II中A的物质的量浓度为m,则M与m的关系为
2C(g),现等物质的量的投料反应物A、B于恒温恒容体系I和恒温、恒压体系II中,达平衡时体系I中A的物质的量浓度为M,体系II中A的物质的量浓度为m,则M与m的关系为
A.M = m B.M > m C.M < m D.以上情况都有可能
打开右图所示装置中的止水夹,一段时间后,可能观察到的现象是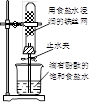
| A.烧杯中有气泡产生 | B.试管内有黄绿色气体产生 |
| C.铁丝网的表面产生锈迹 | D.烧杯内溶液变红色 |