下列各组热化学方程式中,△H1>△H2的是
①C(s)+O2(g)=CO2(g) △H1 C(s)+O2(g)=CO(g) △H2
②S(s)+O2(g)=SO2(g) △H1 S(g)+O2(g)=SO2(g) △H2
③H2(g)+O2(g)=H2O(l) △H1 2H2(g)+O2(g)=2H2O(l) △H2
④CaCO3(s)=CaO(s)+CO2(g) △H1 CaO(s)+H2O(l)=Ca(OH)2(s) △H2
| A.① | B.④ | C.②③④ | D.①②③ |
下列关于价电了构型为3s23p4的粒了描述正确的是
| A.它的元素符号为O |
| B.它的核外电子排布式为1s22s22p63s23p4 |
| C.可以与H2化合生成液态化合物 |
D.其电子排布图为: |
有关核外电予运动规律的描述错误的是
| A.核外电子质量很小,在原子核外作高速运动 |
| B.核外电子的运动规律与普通物体不同,不能用牛顿运动定律来解释 |
| C.在电子云示意图中,通常用小黑点来表示电子绕核作高速圆周运动 |
| D.在电子云示意图中,小黑点密表示电子在核外空间单位体积内电子出现的机会多 |
下列关于主族元素电了排布特征的说法正确的是
| A.主族元素的原子核外电子最后填入的能级是s能级 |
| B.主族元素的原子核外电子最后填入的能级是s能级或p能级 |
| C.主族元素的原子核外电子最后填入的能级是d能级或f能级 |
| D.主族元素的原子核外电子最后填入的能级是s能级或d能级 |
下列关于元素第一电离能的说法不正确的是
| A.钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠 |
| B.对于同一元素而言,原子的逐级电离能越来越大 |
| C.最外层电子排布为ns2np6(若只有K层时为ls2)的原了,第一电离能较大 |
| D.因同周期元素的原了半径从左到右逐渐减小,故第一电离能必依次增大 |
某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1moL•L﹣1NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如图所示,则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为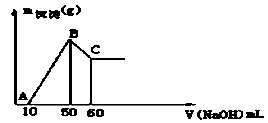
| A.1:1:1 | B.2:1:1 | C.2:2:1 | D.1:1:2 |