下列关于元素第一电离能的说法不正确的是
| A.钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠 |
| B.对于同一元素而言,原子的逐级电离能越来越大 |
| C.最外层电子排布为ns2np6(若只有K层时为ls2)的原了,第一电离能较大 |
| D.因同周期元素的原了半径从左到右逐渐减小,故第一电离能必依次增大 |
在体积为2 L的恒容密闭容器中发生反应xA(g)+yB(g) zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
A.200℃时,反应从开始到平衡的平均速率v(B)=" 0." 02 mol·L-1·min-1
B.图Ⅱ所知反应xA(g)+yB(g) zC(g)的△H<0,且a=2
zC(g)的△H<0,且a=2
C.若在图Ⅰ所示的平衡状态下,再向体系中充入0.2molB和0.2molC,重新达到平衡前v(正)>v(逆)
D.在200℃时,向容器中充入2 mol A 和1 mol B,达到平衡时,A 的体积分数大于0.5
利用如图所示装置进行下列实验,能得出相应实验结论的是
| 选项 |
① |
② |
③ |
实验结论 |
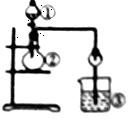 |
| A |
浓盐酸 |
MnO2 |
NaBr溶液 |
氧化性Cl2>Br2 |
|
| B |
浓氨水 |
碱石灰 |
AgNO3溶液 |
AgOH具有两性 |
|
| C |
浓硫酸 |
Na2SO3 |
FeCl3溶液 |
SO2具有还原性 |
|
| D |
稀盐酸 |
Na2CO3 |
Na2SiO3 |
非金属性:C>Si |
液体燃料电池相比于气体燃料电池具有体积小等优点。一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是
| A.b极发生氧化反应 |
| B.a极的反应式:N2H4+4OH--4e-=N2↑+4H2O |
| C.放电时,电流从a极经过负载流向b极 |
| D.其中的离子交换膜需选用阳离子交换膜 |
已知某有机物X的结构简式如图所示,下列有关叙述不正确的是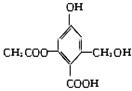
| A.X的化学式为C10H10O6 |
| B.X在一定条件下能与FeCl3溶液发生显色反应 |
| C.1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol |
| D.X在一定条件下能发生消去反应和酯化反应 |
下列实验设计和结论相符的是
| A.在含FeC12杂质的FeCl3溶液中通入足里C12后,充分加热除去过量的C12,即可得到较纯净的FeC13溶液 |
| B.将SO2通入溴水,溴水褪色,说明SO2具有漂白性 |
| C.某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42- |
| D.某溶液中加入NaOH溶液并加热,能产生使湿润红色石蕊试纸变蓝的气体,则一定含有NH4+ |