在体积为2 L的恒容密闭容器中发生反应xA(g)+yB(g) zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
A.200℃时,反应从开始到平衡的平均速率v(B)=" 0." 02 mol·L-1·min-1
B.图Ⅱ所知反应xA(g)+yB(g) zC(g)的△H<0,且a=2
zC(g)的△H<0,且a=2
C.若在图Ⅰ所示的平衡状态下,再向体系中充入0.2molB和0.2molC,重新达到平衡前v(正)>v(逆)
D.在200℃时,向容器中充入2 mol A 和1 mol B,达到平衡时,A 的体积分数大于0.5
下列实验过程中的有关变化与对应的图形相符合的是()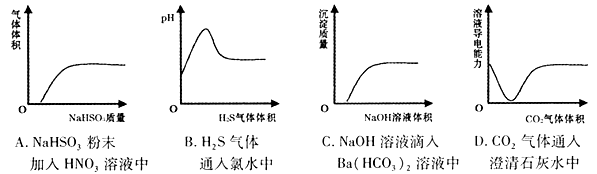
2011年央视3·15特别节目《“健美猪”真相》的报道,将我
国最大肉制品加工企业双汇集团卷入“瘦肉精”漩涡之中。盐酸克伦特罗(即瘦肉精的一种)学名7 – [2 – 甲基丙烷 – 2 – 亚氯基 – 甲基] – 4 – 氨基 – 3,5 – 二氯苯甲醇盐酸盐,是白色或类白色的结晶粉末,无臭,熔点161℃,微溶于丙酮,不溶于乙醚;其结构简式如右。则下列有关说法正确的是()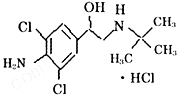
| A.该化合物的分子式C12H18Cl2N2O·HCl |
| B.1mol的该化合物能与2mol的NaOH反应 |
| C.该化合物难溶于水 |
| D.该化合物受热易分解,所以只要将猪肉长时间焖煮即可安全食用 |
下列反应的离子方程式正确的是()
右图是298K、101kPa时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是()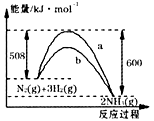
A.该反应的热化学方程式为: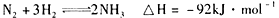 |
| B.a曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热改变 |
| D.在温度、体积一定的条件下,通入1molN2和3molH2反应后 |
放出的热量为Q1kJ,若通入2molN2和6molH2反应后放出的热量
为Q2kJ,则184kJ·mol-1>Q2>2Q1
不能实现下列物质间直接转化的元素的是()
| A.铜 | B.硫 | C.钠 | D.碳 |