“嫦娥一号”卫星上使用的一种高能电池——银锌蓄电池,其电池的电极反应式为:
Zn-2e-+2OH―=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。据此判断氧化银是
| A.负极,被氧化 | B.正极,被还原 | C.负极,被还原 | D.正极,被氧化 |
关于某无色溶液中所含离子的鉴别,下列判断正确的是()
| A.若加入AgNO3溶液,可生成白色沉淀,则可确定该溶液中一定含有Cl-离子 |
| B.若加入Ba Cl 2溶液,能生成白色沉淀,加稀盐酸沉淀不消失,可确定溶液中一定含有SO42-离子 |
| C.验证烧碱溶液中是否含有Cl-,先加盐酸中和烧碱,再加硝酸银溶液,有白色沉淀出现,证明一定有Cl- |
| D.若加入盐酸,生成无色无味的气体且能使澄清的石灰水变浑浊,则原溶液中可能含有大量的HCO3-或者CO32-离子 |
300 mL 0.1 mol/L的AlCl3溶液与200 mL 0.3 mol/L的NaCl溶液中c(Cl-)之比为()
| A.1:1 | B.1:2 | C.1:3 | D.3:2 |
标准状况下,某气体的体积为a L时,它的质量为b g,那么该气体的相对分子质量为()
A.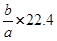 |
B.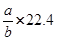 |
C.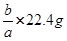 |
D.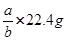 |
同温同压下,相同体积的CO2、CO、H2、O2,质量按从大到小的顺序排列正确的是()
| A.H2>O2>CO>CO2 | B.CO2>O2>CO>H2 |
| C.H2>CO>O2>CO2 | D.CO2>H2>O2>CO |
相等物质的量的CO和CO2的下列比较中正确的是()
①所含的分子数目之比为1:1②所含的O原子数目之比为1:2
③所含的原子总数目之比为2:3④所含的C原子数目之比为1:1
⑤所含的电子数目之比为7:11
| A.①② | B.②③ | C.④⑤ | D.①②③④⑤ |