关于某无色溶液中所含离子的鉴别,下列判断正确的是( )
| A.若加入AgNO3溶液,可生成白色沉淀,则可确定该溶液中一定含有Cl-离子 |
| B.若加入Ba Cl 2溶液,能生成白色沉淀,加稀盐酸沉淀不消失,可确定溶液中一定含有SO42-离子 |
| C.验证烧碱溶液中是否含有Cl-,先加盐酸中和烧碱,再加硝酸银溶液,有白色沉淀出现,证明一定有Cl- |
| D.若加入盐酸,生成无色无味的气体且能使澄清的石灰水变浑浊,则原溶液中可能含有大量的HCO3-或者CO32-离子 |
一定温度下,将2mol A、2mol B、2mol C的气体混合物充入一体积不变密闭容器中,充分反应后恢复到起始温度,测得容器内的压强比起始时增大了20%,则容器中可能发生的反应是
A.2A+B 2C B.A+B
2C B.A+B 2C C.2A+B
2C C.2A+B C D.2A+B
C D.2A+B 4C
4C
反应 A+B→C 的反应速率方程式为:v=k c (A) c (B),v为反应速率,k为速率常数。当c (A)=c (B)=1mol/L时,反应速率在数值上等于速率常数。下列说法正确的是
A.只增大c (A)时,v也增大 B.只增大c (A)时,v值不变
C.只升高温度时,k值不变 D.只升高温度时,k值变小
在0.lmol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
| A.加入少量NaOH固体,平衡向正反应方向移动 |
| B.加水,反应速率增大,平衡向逆反应方向移动 |
| C.滴加少量0.lmol/L HCl溶液,溶液中c(H+)减少 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
有下列五个化学方程式(X、Y、Z均为正值):
①C2H2(g)+H2(g) C2H4(g)
C2H4(g)
②CH4(g) H2(g)+
H2(g)+ C2H4(g)
C2H4(g)
③C(s)+2H2(g) CH4(g);△H=-X kJ·mol—1
CH4(g);△H=-X kJ·mol—1
④C(s)+ H2(g)
H2(g)
 C2H2(g);△H=-Y kJ·mol—1
C2H2(g);△H=-Y kJ·mol—1
⑤C(s)+H2(g)
 C2H4(g);△H=-Z kJ·mol—1
C2H4(g);△H=-Z kJ·mol—1
当温度下降时①式平衡向右移动,②式平衡向左移动。据此判定③—⑤式中关于X、Y、Z的大小顺序排列正确的是
| A.X>y>Z | B.X>Z>Y | C.Y>X>Z | D.Z>X>Y |
某温度下在密闭容器中发生如下反应:2SO2+O2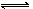 2SO3(g),若开始时只充入2 molSO3(g),达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入了2 mol SO2和1 molO2的混合气体,达到平衡时SO2的转化率为
2SO3(g),若开始时只充入2 molSO3(g),达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入了2 mol SO2和1 molO2的混合气体,达到平衡时SO2的转化率为
| A.20% | B.40% | C.50% | D.60% |