某温度下,浓度都是1.0mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z。10min后测得X2、Z的浓度分别为0.4mol/L、0.6mol/L,则该反应的化学方程式可能为
A.X2+2Y2 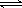 2XY2 2XY2 |
B.3X2+Y2 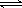 2X3Y 2X3Y |
C.2X2+Y2 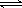 2X2Y 2X2Y |
D.X2+3Y3 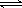 2XY3 2XY3 |
鉴别织物成分是真丝还是人造丝,正确的操作方法是
| A.滴加醋酸 | B.滴加浓硫酸 |
| C.滴加酒精 | D.灼烧 |
19世纪中叶,门捷列夫的突出贡献是
| A.提出原子学说 | B.发现元素周期律 |
| C.提出分子学说 | D.发现并制备氧气 |
下列物质能作为食品添加剂的是
| A.苏丹红 | B.三聚氰胺 | C.味精 | D.瘦肉精 |
防治酸雨是一项综合性工程,下列叙述不正确的是
| A.研究开发替代化石燃料的新能源 |
| B.对含硫燃料预先进行脱硫处理 |
| C.加强国际间合作,以减少酸雨的产生 |
| D.将烟囱建得更高些,避免SO2排放在本地 |
在航天飞机返回地球大气层时,为防止其与空气剧烈摩擦,产生高温(1000℃以上)而被烧毁,需在航天飞机外表面安装保护层。该保护层的材料可能是
| A.铝合金 | B.合成纤维 |
| C.耐高温新型陶瓷 | D.塑料钢 |