X、Y、Z、W四种元素在元素周期表中序数逐渐增大。X为非金属元素,且X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)Z的元素原子结构示意图是: ,位于周期表中第_____周期第 族;
(2)有X、Y、Z所形成的离子化合物是 ,它与W的最高价氧化物对应水化物的溶液加热时反应的离子方程式是 ;
(3)Y的单质的电子式为 ,结构式为 ,其中的化学键属于 键(填“离子”或“共价”)。
已知可逆反应CO(g)+H2O(g) 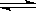 CO2(g)+H2(g),达到平衡时,K=
CO2(g)+H2(g),达到平衡时,K=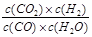 ,K是常数,只与温度有关,与浓度无关。
,K是常数,只与温度有关,与浓度无关。
(1)830K时,若起始时c(CO)="2" mol·L-1,c(H2O)="3" mol·L-1,平衡时CO的转化率为60%,水蒸气的转化率为;K值为。
(2)830 K时,若只将起始时c(H2O)改为6 mol·L-1,则水蒸气的转化率为。
(3)若830 K时,起始浓度c(CO)="a" mol·L-1,c(H2O)="b" mol·L-1,H2的平衡浓度c(H2)="c" mol·L-1①a、b、c之间的关系式是;②当a=b时,a=c。
按下图装置进行实验,并回答下列问题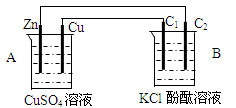
(1)判断装置的名称:A池为B池为
(2)铜极为______极,电极反应式为
(3)B装置中,C1与C2均为石墨棒,石墨棒C1为___极,电极反应式为,石墨棒C2附近发生的实验现象为
(4)当C2极析出224mL(标准状态)气体时,锌的质量减少g.
把一根卷成螺旋状的铜丝在酒精灯火焰上加热,红色的铜丝变成色,把它立即插入盛有乙醇的试管中,铜丝表面出现的变化是;重复几次同样的操作,试管内液体散发出具有刺激性气味的气体,这是乙醇被而生成之故。在反应后的试管中加入适量的新制氢氧化铜悬浊液,再加热至沸,可发现试管中的混和物中有生成。(以上每空1分)发生该反应的化学方程式。
某烃A 0.2mol在氧气中充分燃烧后,生成化合物B、C各1.2mol。试回答:
(1)烃A的分子式为。
(2)若取一定量的烃A完全燃烧后,生成B、C各3mol,则有g烃A参加了反应,燃烧时消耗标准状况下的氧气L。
(3)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则此烃A的结构简式为。
(4)若烃A能使溴水褪色,在催化剂作用下,与氢气加成,其加成产物经测定分子中含有4个甲基。烃A可能有的结构简式为。
如图是常见原电池装置,电流表G发生偏转: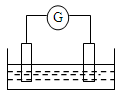
(1)若两个电极分别是Zn、Cu,电解质溶液是稀硫酸,正极的电极反应式为___________________________;如果把电解质溶液换成硫酸铜溶液,则正极的电极反应式为_____________________________。
(2)若总反应是2FeCl3+Fe=3FeCl2,则可以做负极材料的是________,
负极上发生的电极反应是________________________。
(3)若电解质溶液是稀硫酸,Mg、Al两种金属做电极,则Mg电极的电极反应式为_____________;
若电解质溶液换作稀氢氧化钠溶液,Mg、Al两金属做电极,则Mg是____(填“正极”或“负极”),总反应的离子方程式是_______________________________。