下列有关同位素的说法正确的是
| A.电子数相同,中子数不同的两种微粒 |
| B.质子数相同,中子数不同的两种原子 |
| C.质子数相同,中子数不同的两种离子 |
| D.质量数相同,中子数不同的两种原子 |
四种主族元素的离子aXm+、bYn+、cZn-和dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,则下列叙述正确的是( )。
①a-b=n-m ②元素的原子序数:a>b>c>d ③元素非金属性:Z>R ④最高价氧化物对应的水化物的碱性:X>Y
| A.只有③ | B.①②③④ | C.①②③ | D.②③ |
已知铍的原子序数为4,下列对铍及其化合物的叙述中,正确的是( )。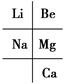
| A.铍的金属性比钠强 |
| B.氯化铍的氧化性比氯化锂弱 |
| C.氢氧化铍的碱性比氢氧化钙弱 |
| D.单质铍易跟冷水反应生成H2 |
元素X、Y、Z的原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子排布。下列推测不正确的是( )。
| A.同周期元素中X的金属性最强 |
| B.原子半径:X>Y,离子半径:X+>Z2- |
| C.同族元素中Z的氢化物稳定性最高 |
| D.同周期元素中Y的最高价含氧酸的酸性最强 |
有人建议将氢元素排在元素周期表的ⅦA族。下列事实能支持这一观点的是( )。
①H原子得到一个电子实现最外电子层稳定结构;
②氢分子的结构式为H—H;
③与碱金属元素形成离子化合物:M+[:H]-
④分子中原子间的化学键都属于非极性键
| A.①②③ | B.①③④ | C.②③④ | D.①②③④ |
A、B、C、D、E是同周期的五种主族元素。A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A;C和D的最高价氧化物对应的水化物均呈酸性,且酸性C>D,E是这五种元素中原子半径最小的元素,它们的原子序数由小到大的顺序是( )。
A.A<B<C<D<E B.C<D<A<B<E
C.B<A<D<C<E D.E<C<D<B<A