有机化合物A~H的转换关系如下所示: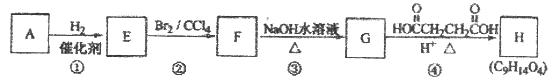
请回答下列问题:
(1)链烃A有支链且只有一个官能团,其相对分子质量为68,则A的分子式为 ,结构简式是 :
(2)在特定催化剂作用下,A与等物质的量的H2反应生成E。由E转化为F的化学方程式是 ;
(3)①的反应类型是 ;③的反应类型是
(4)G与金属钠反应能放出气体,由G转化为H的化学方程式是
(11分)肉桂酸甲酯是一种常用的调制具有水果香味的食用香精。下图是由A合成聚肉桂酸甲酯等有机物的合成信息:
已知:

②F为由两分子D间反应形成含有三个六元环的酯;

请回答下列问题:
(1)D→G的反应类型是________________;G→H的反应类型是________________;
(2)D转化为E的化学方程式是______________________________________________;
(3)下列物质的结构简式:A_______________________________;F________________;
(4)符合以下条件的D的同分异构体有_____种,写出其中一种的结构简式________________。
①苯环上有2种氢,3个取代基; ②能发生银镜反应; ③遇FeCl3溶液显色。
(5)请用合成路线流程图表示 →G的合成线路,并注明反应条件。
→G的合成线路,并注明反应条件。
提示:①氧化羟基的条件足以氧化有机分子中的碳碳双键;
②合成过程中无机试剂任选;
③合成路线流程图示例如下:
X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:
| X |
Y |
Z |
M |
R |
Q |
|
| 原子半径/nm |
0.186 |
0.074 |
0.099 |
0.143 |
||
| 主要化合价 |
-4,+4 |
-2 |
-1,+7 |
+3 |
||
| 其它 |
阳离子核外无电子 |
无机非金属材料的主角 |
焰色反应呈黄色 |
(1)R在元素周期表中的位置是________________;R在自然界中有质量数为35和37的两种核素,它们之间的关系互为________________。
(2)Z的单质与水反应的离子方程式是_________________________。
(3)根据表中数据推测,Y的原子半径的最小范围是________________。
(4)Z、M、Q的简单离子的离子半径的大小顺序为________________。
(5)Y与R相比,非金属性较强的是________________(用元素符号表示),下列事实能证明这一结论的是________________(选填字母序号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR >YX4
c.Y与R形成的化合物中Y呈正价
(6)甲、乙是上述部分元素的最高价氧化物的水化物,且甲+乙→丙+水。若丙的水溶液呈碱性,则丙的化学式是_______________________________。
(7)Y的单质能和Z的最高价氧化物的水化物的水溶液发生反应,生成相同条件下密度最小的气体。请写出该反应的化学方程式_____________________。
有一无色溶液,可能含有K+、A13+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入盐酸酸化的BaCl2溶液,有白色沉淀产生。根据上述实验现象回答下列问题。
(1)其中肯定含有的离子有:________________,无法确定是否含有的离子有:________________。
(2)写出溶液加入适量Na2O2固体,产生无色无味气体的离子反应方程式___________________________。
(3)简述产生白色沉淀在加入足量的NaOH溶液后白色沉淀发生部分溶解现象的原因 ________________________________________________________________________。
(7分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
NO3—+4H++3e—→NO+2H2O KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出该氧化还原反应的离子方程式:________________________________。
(2)反应中硝酸体现的性质有_________、__________。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是________________mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是: _______________________________________________________________________。
2 g Cu2S和CuS的混合物在酸性溶液中用400mL 0.075 mol/L KMnO4溶液处理,反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的 KMnO4恰好与350 mL 0.1 mol/L (NH4)2Fe(SO4)2溶液完全反应,反应的离子方程式:MnO4-+5Fe2++8H+=Mn2++5 Fe3+ +4H2O
(1) KMnO4溶液与混合物反应,消耗KMnO4的物质的量为mol。
(2)欲配制500mL 0.1mol/L NH4+溶液,需称取 (NH4)2Fe(SO4)2·6H2O (M=392g/mol)的质量为 g。
(3)混合物中 Cu2S的质量分数为 。