如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片。经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面。以下有关解释合理的是
| A.生铁片中的碳是原电池的负极,发生还原反应 |
| B.雨水酸性较强,生铁片始终发生析氢腐蚀 |
| C.墨水液面回升时,生铁片发生吸氧腐蚀 |
| D.U型管中溶液pH逐渐减小 |
三硫化四磷用于制造火柴及火柴盒摩擦面,分子结构如下图所示。下列有关三硫化四磷说法中正确的是
| A.该物质中磷元素的化合价为+3 |
B.该物质分子中含有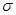 键和 键和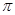 键 键 |
| C.该物质的熔、沸点比食盐高 |
| D.该物质22g含硫原子的数目约为1.806×1023 |
相同温度,浓度均为0.1mol /L,等体积的三种溶液:①HF溶液、②CH3COOH溶液、③NaHCO3溶液,已知将①、②分别与③混合,实验测得产生的CO2气体体积(v)随时间(t)的变化如右图所示,下列说法正确的是( )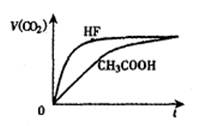
| A.上述三种溶液中:c( OH-)大小:③ > ② > ① |
| B.物质酸性的比较:CH3COOH > HF > H2CO3 |
| C.反应结束后所得两溶液中: c ( CH3COO- ) > c ( F- ) |
| D.①和③反应结束后所得溶液中:c ( F- ) + c (HF) =" 0.10mol" /L |
用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4 (g) + 2N2 (g) + 6H2 (g)  Si3N4(s) + 12HCl (g)∆H < 0
Si3N4(s) + 12HCl (g)∆H < 0
该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
| 选项 |
x |
y |
| A |
温度 |
容器内混合气体的密度 |
| B |
N2 的物质的量 |
H2的转化率 |
| C |
H2的浓度 |
平衡常数K |
| D |
压强 |
N2 的转化率 |
化学家正在研究尿素动力燃料电池,尿液也能发电。用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,下列关于描述正确的是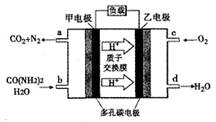
| A.电池工作时H+ 移向负极 |
| B.该电池用的电解质溶液是KOH溶液 |
| C.甲电极反应式为:CO(NH2 )2 +H2O - 6e-= CO2 +N 2 + 6H+ |
| D.电池工作时,理论每有净化1mol CO(NH2 )2,消耗 33.6 L O2 |
下列叙述的实验能达到预期目的的是( )
| 选项 |
实验内容 |
实验目 |
| A |
滴定实验中,用待测液润洗锥形瓶2~3次 |
避免造成实验误差 |
| B |
向氯水滴加AgNO3、稀HNO3溶液,产生白色沉淀 |
验证氯水中含有Cl- |
| C |
向盛有沸水的烧杯中滴加饱和氯化铁溶液并长时间煮沸 |
制备氢氧化铁胶体 |
| D |
向2mL 1mol· L-1 NaOH溶液中先加入3滴1mol· L-1 MgCl2溶液,再加入3滴1mol· L-1 FeCl3溶液 |
证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 |