下表是KNO3、NaCl在不同温度下的溶解度(单位:g):
| 温度(℃) |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
| KNO3 |
20.9 |
32 |
45.8 |
64 |
85.5 |
110 |
138 |
169 |
| NaCl |
35.8 |
36 |
36.3 |
36.6 |
37 |
37.3 |
37.8 |
38.4 |
(1)以上两种物质溶解度的变化受温度影响较小的是 。
(2)20℃时,食盐饱和溶液中溶质的质量分数是 。(保留一位小数)
(3)用上表数据来画溶解度曲线,两种物质的曲线相交时的温度范围应是 。(填字母序号)
A.10~20℃ B.20~30℃ C.30~40℃ D.40~50℃
(4)70℃时,将138gKNO3、37gNaCl分别溶解在各装有100g水的两个烧杯中,其中能形成饱和溶液的是 ;若从70℃降到20℃后,下列说法中正确的是 (填字母序号)。
A.KNO3析出,NaCl不析出
B.其溶剂的质量不变
C.KNO3和NaCl的质量分数都降低
D.KNO3的质量分数降低,NaCl的质量分数不变
碳和碳的氧化物,是自然界庞大的家族,回答下列问题:
金刚石和石墨物理性质差异的原因为 ,由石墨制成金刚石属于 变化,
一氧化碳和二氧化碳二者的化学性质相差甚远,理由是:
我国古代一些书法家、画家用墨书写或绘制的字画能够保存很长时间而不变色,这是因为单质碳具有
除去CO2中混有的少量CO,方法是
试管中盛有黑色粉末,将其加强热,粉末变为红色,同时产生无色气体,该气体能使澄清的石灰水变浑浊,则这两种黑色物质反应的化学方程式是
“碳海绵”是已知最轻的固体材料,主要成分是石墨烯和碳纳米管,具有疏松多孔结构.它对石油有很强的吸附能力,将吸人的石油挤出后仍可恢复原状.下列关于碳海绵的说法不正确的是 .
| A.具有吸附性 |
| B.可重复使用 |
| C.可处理海上泄漏的石油 |
| D.碳海绵是灰黑色固体 |
E.碳海绵易溶解于水
F.碳海绵燃烧会产生二氧化碳.
已知A~F都是初中化学中的常见物质, A为黑色固体单质,C是无色无味气体,能是澄清石灰水变浑浊, D是红色固体,C→E是自然界中最常见的转化。物质间的转化关系如图所示: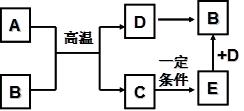
(1)写出下列物质的化学式:B _________, E _________;
(2)写出A与B反应的化学方程式:_________________________
如图是初中化学中常用的实验装置,请回答下列问题。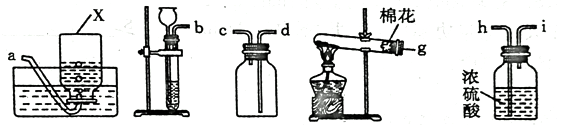
A B C D E
(1)仪器X的名称是 。
(2)实验室制取O2、CO2均可选择 (填装置代号)作为气体的发生装置。
(3)实验室不使用催化剂就能制取O2的反应化学方程式为 ________________;
(4)请从这些装置中选择并连接成一套组合装置,用于实验室制取干燥的CO2气体。按照气体从左至右的流向,写出所选装置接口的连接顺序:
( )→( )→( )→( )→( )
见著知微,见微知著”是化学思维方法。根据以下微观粒子,回答下列问题
①微粒A在化学反应中容易___________(填“得”或“失”)电子;
②微粒A、B、C、D、E中,对应单质化学性质最稳定的是______________(填编号,下同),属于同一种元素的是_________________和______________。
用化学符号填写下列空格
(1)五氧化二磷 (2)硫酸锌中锌元素的化合价显+2价
(3)4个铜离子 (4)人体中含量最高的金属元素__________