在密闭容器中发生如下反应:mA(g)+nB(g) pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是
| A.m+n<p | B.平衡向逆反应方向移动 |
| C.A的转化率降低 | D.C的体积分数增加 |
在恒温、恒容下,发生如下反应:2A(g)+2B(g) C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2mol/L;Ⅱ途径:C、D的起始浓度分别为2mol/L和6mol/L。以下叙述正确的是 ()
C(g)+3D(g),现从两条途径分别建立平衡。途径Ⅰ:A、B的起始浓度均为2mol/L;Ⅱ途径:C、D的起始浓度分别为2mol/L和6mol/L。以下叙述正确的是 ()
A.达平衡时,途径Ⅰ的反应速率V(A)等于途径Ⅱ的反应速率V(A)
B.达平衡时,途径Ⅰ所得混合气的浓度和途径Ⅱ所得混合气体的浓度相等
C.两途径最终达到平衡时,体系内混合气体的百分组成不同
D.两途径最终达到平衡时,体系内混合气体的百分组成相同
在一密闭容器中,反应aA(气) bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则()
bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则()
| A.平衡向逆反应方向移动了 | B.物质B的质量分数增加了 |
| C.物质A的转化率减少了 | D.a>b |
下列事实中不能用勒夏特列原理加以解释的是()
| A.压缩氢气与碘蒸气反应的平衡混合气体,颜色变深 |
| B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体 |
| C.夏天,打开啤酒瓶时会在瓶口逸出气体 |
| D.将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅 |
在一密闭烧瓶中,在25℃时存在着平衡:

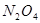 (正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是( )
(正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是( )
①颜色; ②平均相对分子质量;③质量;④压强;⑤密度
| A.①和③ | B.②和④ | C.③和⑤ | D.④和⑤ |
下列对化学平衡移动的分析中,不正确的是 ()
(1)已达平衡的反应

 ,当增加反应物物质的量时,平衡一定向正反应方向移动
,当增加反应物物质的量时,平衡一定向正反应方向移动
(2)已达平衡的反应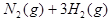

 ,当增大
,当增大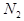 的浓度时,平衡向正反应方向移动,
的浓度时,平衡向正反应方向移动,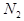 的转化率一定升高
的转化率一定升高
(3)有气体参加的反应达平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
(4)有气体参加的反应达平衡后,在恒压反应器中充入稀有气体,平衡一定不移动
| A.(1)(4) | B.(1)(2)(3) |
| C.(2)(3)(4) | D.(1)(2)(3)(4) |