下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100 5.00%的
5.00%的 溶液、足量的
溶液、足量的 溶液和l00
溶液和l00 10.00%的
10.00%的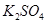 溶液.电极均为石墨电极。接通电源,经过一段时间后,测得丙中
溶液.电极均为石墨电极。接通电源,经过一段时间后,测得丙中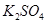 浓度为10.47%,乙中c电极质量增加。据此回答问题:
浓度为10.47%,乙中c电极质量增加。据此回答问题:

①电源的N端为 极;
②电极b上发生的电极反应为 ;
③电极b上生成的气体在标准状况下的体积: ;④电极c的质量变化是  ;
;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液 ;
乙溶液 ;
丙溶液 ;
下表所列物质(括号内为少量杂质),在B中选择试剂,在C中选择操作的方法。填表(填入序号):
B:(1)CaO;(2)NaOH溶液;(3)溴水; (4)饱和Na2CO3;(5)水
C:(1)重结晶;(2)洗气;(3)蒸馏(4)分液。
| 物质 |
加入试剂 |
操作方法 |
| ①粗苯甲酸的提纯 |
||
| ②乙醇(水) |
||
| ③乙酸乙酯(乙酸) |
||
| ④乙烷(乙烯) |
||
| ⑤苯(酒精) |
已知某有机物的结构简式为:
(1)该有机物中所含官能团的名称是__、__。
(2)该有机物发生加成聚合反应后,所得产物的结构简式为__。
(1)双酚A是食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大。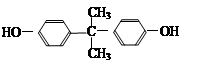
双酚A的核磁共振氢谱显示氢原子数之比是
(2)对羟基扁桃酸是农药、药物、香料合成的重要中间体, 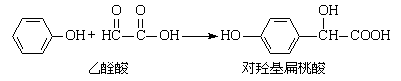
在核磁共振氢谱中对羟基扁桃酸应该有组吸收峰
当0.2mol烃A在足量氧气中完全燃烧时生成CO2和H2O各1.2mol,催化加氢后生成2,2-二甲基丁烷,则
(1)A的结构简式为,(2)A的命名为:。
在有机物:①CH3CH3、②CH2=CH2、③CH3CH2C≡CH、④CH3C≡CCH3、⑤C2H6、⑥CH3CH=CH2中,一定互为同系物的是,一定互为同分异构体的是。(填编号)