某化学实验兴趣小组在“探究氯水与溴化亚铁溶液反应”的实验中发现:“在足量的溴化亚铁溶液中,加入1~2滴氯水,振荡后溶液呈黄色。”
| 【资料】 |
溴水是溴单质的水溶液,因溶有溴单质而呈黄色。 |
根据已有化学知识及资料,请你参与上述现象形成原因的分析与探究:
(1)提出问题猜想:
溶液呈黄色是因发生离子反应① (填离子方程式)所致。
溶液呈黄色是因发生离子反应② (填离子方程式)所致。
(2)设计实验并验证
为验证①与②中是哪个原因导致了溶液变黄色,设计并进行了以下实验。请根据以下所给试剂,进行合理选用,完成实验方案1和方案2:
| 试剂 |
酚酞试液、CCl4、无水酒精、KSCN溶液 |
||
| 方案 |
操作步骤 |
实验现象 |
结论 |
| 1 |
取所述黄色溶液于试管中,滴加 并振荡 |
溶液变红色 |
反应 所致 |
| 2 |
取所述黄色溶液于试管中,滴加 并振荡 |
________ ________ |
(3)实验结论:以上实验不仅验证了溶液变黄的真实原因,同时证明了Fe2+的还原性比Br- (填“强”或“弱”)。
(4)实验反思
I. 根据上述实验推测,若在溴化亚铁溶液中滴入足量氯水,再加入CCl4并充分振荡后静止,产生的现象是 。
Ⅱ. 在100 mLFeBr2溶液中通入2.24 L Cl2(标准状况),溶液中有1/2的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 。
(共22分)某实验小组用下列装置进行如下的实验。
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式
、。
实验小组在不断鼓入空气的情况下,熄灭酒精灯,发现反应仍能继续进行,说明该反应是 反应。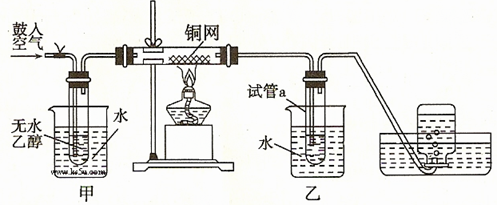
(2)甲和乙两个水浴作用不相同。甲的作用是;
乙的作用是。
(3)反应进行一段时间后,干燥的試管a中能收集到不同的物质,那么收集到的有机物是(请填写其结构简式);集气瓶中收集到的气体的最主要成分是。(填写气体的分子式)
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,实验小组的同学认为这可能是存在副产物乙酸。除去该物质,可以使用厨房中常见的一种化合物,该物质为 。(填写化学式或分子式)
。(填写化学式或分子式)
(5)请写出以上实验涉及的有机物乙醇在生活生产中的一种具体应用:。
(6)该实验的目的是:
某实验小组用下列装置进行乙醇催化氧化的实验。已知:乙醛可被氧化为乙酸。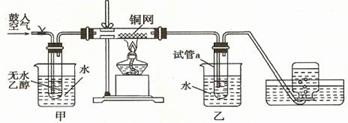
⑴实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式___________________。
⑵在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应
是反应。
⑶若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有。要除去该物质,可在混合液中加入(填写字母)。
| A.氯化钠溶液 | B.苯 | C.碳酸氢钠溶液 | D.四氯化碳 |
然后,再通过(填实验操作名称)即可除去。
下图是实验室制取乙酸乙酯的实验装置。请回答:
(1)在M试管中加碎瓷片的作用是。
试管N中盛放的溶液是_________________ 。
该溶液的作用为中和乙酸,吸收挥发出的乙醇,;
导管在其 液面上而不插入液面下的原因是。
(2)在大试管中配制一定比例的乙醇、浓硫酸和乙酸
混合液时,加入试剂的顺序是。
(3)浓硫酸的作用是。
(4)反应结束后,试管N内的液体分成两层,反应生成的乙酸乙酯在层(填写“上”或“下”)。若分离N中的液体混合物需要用到的玻璃仪器是烧杯、。
(5)M试管中发生反应的化学方程式。
(6)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,
就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯
化反应已达到化学平衡状态的是 (填序号)。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
如图装置可以用来制取某些气体。
(1)该装置可以制备乙炔气体,圆底烧瓶中盛放的物质是(填化学式)。
(2)还能用该装置制备和收集的气体有(答出任意一种即可)。
(3)若用来制备乙烯气体,需要对装置进行改进,将分液漏斗改成温度计,温度计的水银球放置的位置是,改进时还需要的玻璃仪器是;反应的化学方程式是。
某实验小组用下列装置进行乙醇催化氧化的实验。已知:乙醛可被氧化为乙酸。
⑴实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式______________________、______________________。
⑵在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应
是反应。
⑶若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有。要除去该物质,可在混合液中加入 (填写字母)。
| A.氯化钠溶液 | B.苯 | C.碳酸氢钠溶液 | D.四氯化碳 |
然后,再通过(填实验操作名称)即可除去。