请回忆你和老师共同完成的酸和碱反应的实验探究,并按下列要求进行实验设计与分析:
【实验探究】
⑴请你依据下图设计一个酸和碱反应的探究实验: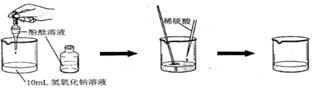
| 实验步骤 |
实验现象 |
结论 |
| ①向烧杯中加入10mL氢氧化钠溶液,并滴入几滴酚酞试液 |
①溶液颜色 ; |
酸和碱发生了中和反应 |
| ②再用滴管慢慢滴入稀硫酸,并不断搅拌溶液。 |
②不断搅拌溶液至溶液颜色变成 色。 |
⑵为探究上述酸、碱反应后硫酸是否过量,甲、乙、丙三位同学设计了以下方案:
| 实验方案 |
实验步骤 |
实验现象 |
实验结论 |
| 甲同学的方案 |
取样,滴入适量的氯化钡溶液 |
出现白色沉淀 |
硫酸过量 |
| 乙同学的方案 |
取样,滴入几滴无色酚酞溶液 |
酚酞溶液不变色 |
酸、碱恰好完全反应 |
| 丙同学的方案 |
取样,滴入几滴紫色石蕊溶液 |
溶液变红 |
硫酸过量 |
【实验评价】
①设计的三个方案中,有一个正确的方案,是 (填“甲”、“乙”、“丙”)同学的方案
②请分析另外两个同学方案错误的原因:
一个同学方案错误的原因是 ,
另一个同学方案错误的原因是 。
【实验反思】探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂
实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的文字表达式:
。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
[提出猜想]除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
[完成实验]按下表进行实验,并测定分解温度(分解温度越低,催化效果越好)。
| 实验编号 |
实验药品 |
分解温度(℃) |
| ① |
氯酸钾 |
580 |
| ② |
氯酸钾、二氧化锰(质量比1:1) |
350 |
| ③ |
氯酸钾、氧化铜(质量比1:1) |
370 |
| ④ |
氯酸钾、氧化铁(质量比1:1) |
390 |
[分析数据、得出结论](1)由实验与实验④对比,证明猜想合理;
(2)实验所用的三种物质,催化效果最好的是。
[反思](3)若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的质量和
不变;
将过量的Na2CO3溶液滴入到一定量CuSO4溶液中得到蓝色固体。某研究性学习小组对固体沉淀的成分进行了如下探究。请完成下列各题:
(一)猜想与假设:
猜想一:固体为CuCO3,理由:(用化学反应方程式表示)。
猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈(填“酸”或“碱”)性。
猜想三:固体为Cu(OH)2和CuCO3的混合物。
(二)资料查阅:
①结晶水合物受热后易失去结晶水,如CuSO4•5H2O CuSO4 + 5H2O↑;
CuSO4 + 5H2O↑;
②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物。
③无水氯化钙可做吸水剂;碱石灰的主要成分为氢氧化钠固体和氧化钙
(三)设计与实验:
Ⅰ.固体的获取:
(1)将反应后的固、液混合物经、洗涤、室温晾干得蓝色固体。
Ⅱ.用下图所示方案,初步定性探究固体的成分。 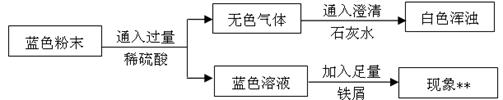
(2)无色气体为
(3)加入足量铁屑发生反应的方程式为、
结论:猜想不成立。
Ⅲ.固体组成定量测定:
设固体为aCu(OH)2•bCuCO3•cH2O,为测定其组成,称取24.0 g蓝色固体。继续进行实验:
【实验步骤】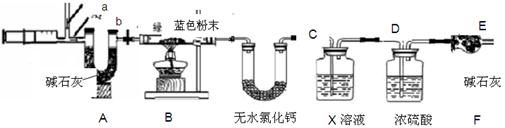
图中注射器处为两个单向阀:推注射器时a关闭,b处打开;拉注射器时,a打开进空气,b关闭。
实验步骤 ①组装好装置,检查气密性;②反复推拉注射器;③称量B、C、D、E、F的质量;④关闭弹簧夹,加热B处试管直到反应不再进行;⑤打开弹簧夹,再次反复缓缓推拉注射器;⑥再次称量B、C、D、E、F的质量。
问题探究:
(4)写出Cu(OH)2、CuCO3分解的化学方程式、。
样品分解的总反应方程式。
说明装置B中样品没有完全反应的现象是
(5)D中的药品为,作用是。
(6)进行步骤⑤的操作,是为了,该操作中推注射器时缓缓的目的是。
数据处理:
| B |
C |
D |
E |
F |
|
| 反应前 |
124.0g |
250.0g |
300.0g |
350.0g |
360.0g |
| 反应后 |
116.0g |
253.6g |
304.2g |
350.2g |
360.0g |
(7)据下表数据,E装置质量增加的原因是;24.0g固体分解出水的质量为g,;
(8)求该固体的化学式中 a:b:c=。(写出计算过程,4分)
探究实验报告一:蜡烛及其燃烧的探究
探究实验的名称:蜡烛及其燃烧的探究
探究实验的目的:理解掌握蜡烛的有关性质知识
实验用品:蜡烛、火柴、等
| 步骤和方法 |
现象 |
分析 |
|
| 点燃前 |
蜡烛是白色蜡状固体,硬度小,稍有气味 |
||
| 用小刀切下一小块蜡烛投入水中 |
石蜡浮于水面 |
||
| 点燃蜡烛 |
蜡烛先熔化后气化,再燃烧;火焰明亮且明显分成三层 |
||
| 在烛焰上方罩一干燥烧杯 |
烧杯内壁出现水雾或水珠 |
||
| 在烛焰上方罩一个内壁沾有澄清石灰水的烧杯,振荡 |
烧杯内壁出现白色斑点 |
||
| 熄灭蜡烛 |
火焰熄灭,灯芯上产生一缕轻烟 |
轻烟为蜡烛蒸气冷却所致,遇明火可以燃烧。 |
结论:在通常情况下,蜡烛是白色蜡状固体,稍有气味,熔点、熔点较低,硬度较小,密度比水小。蜡烛在点燃条件下能燃烧,燃烧产物中有水和二氧化碳等。
问题和建议:为进一步说明蜡烛是先气化,然后是石蜡蒸气燃烧,可用一根尖嘴的细玻璃管插入焰心,然后在尖嘴处点燃。根据是否能点燃,可推断上述猜测是否正确。
在化学实验室,小刚和小强意外发现实验桌上有一瓶敞口放置的氢氧化钠固体,他们对这瓶氢氧化钠固体是否变质进行了如下实验探究:
【提出问题】这瓶氢氧化钠固体是否变质?
氢氧化钠露置在空气中会发生变质。变质的原因是(用化学方程式表示)。
【实验探究】为检验这瓶氢氧化钠固体是否变质,小刚和小强设计了如下实验方案:
小刚:取少量样品加适量蒸馏水配成溶液后,滴人几滴酚酞溶液,若观察到溶液变红色,证明该瓶氢氧化钠固体没有变质。
小强:取少量样品加适量蒸馏水配成溶液后,滴入适量澄清石灰水,若观察到有白色沉淀生成,证明该瓶氢氧化钠固体已经变质。
你认为上述实验方案错误的是.
理由是.
请你设计另外一个方案,证明该瓶氢氧化钠固体已经变质,并完成以下实验报告:
| 实验步骤 |
实验现象及结论 |
【交流反思】在实验室里氢氧化钠需要密封保存。药品密封保存的原因很多,请你写出浓硫酸需要密封保存的原因。
某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:
),这种工业称为"氯碱工业"。某研究性学习小组对该厂生产的烧碱样品进行如下探究。
I.定性探究
【提出问题】烧碱样品中可能含有哪些杂质?
【猜想】猜想一:可能含有
,作出此猜想的依据是(用化学方程式表示)。
猜想二:可能含有
,作出此猜想的依据是(用简洁的文字表述)。
【设计实验】
| 实验步骤 |
实验现象 |
解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁。 |
试管外壁发热 |
原因是 |
| ②向①所得的溶液中逐滴加入稀硝酸至过量 |
一开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体。 |
样品中含有的杂质是 |
| ③向②所得的溶液中滴加几滴硝酸银溶液 |
产生白色沉淀 |
样品中还含有的杂质是 |
【交流与讨论】小明同学提出:"上述实验中稀硝酸也可以用稀盐酸代替"。你认为他的观点
(填"正确"或"不正确")。
II.定量探究
【提出问题】烧碱样品中氢氧化钠的质量分数是多少呢?
【设计实验】小婉同学设计探究方案后进行实验并测得数据如下:
请你利用小婉同学测得的数据计算烧碱样品中氢氧化钠的质量分数(请列出计算过程)。
【交流与反思】小强同学认为小婉同学设计的探究方案不够严密,其理由是:
(1)探究方案中未考虑氢氧化钠的吸水性。
(2)探究方案中因缺少(填操作名称),导致测得的氢氧化钠的质量分数偏小。