下列各离子①R- ②R+ ③ R3+④RH4+ ⑤ RH-(R表示不同的元素)都有10个电子,其中不会破坏水的电离平衡的有( )
| A.仅有② | B.①②③ | C.②③④ | D.①②⑤ |
一些烷烃的标准燃烧热如下表:
| 化合物 |
标准燃烧热(△H/KJ·mol-1) |
化合物 |
标准燃烧热(△H/KJ·mol-1) |
| 甲烷 |
-891.0 |
正丁烷 |
-2878.0 |
| 乙烷 |
-1560.8 |
异丁烷 |
-2869.6 |
| 丙烷 |
-2221.5 |
2-甲基丁烷 |
-3531.3 |
下列说法正确的是
A.热稳定性:正丁烷>异丁烷
B.正戊烷的标准燃烧热大约为:△H=一3540kJ/mol
C.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)→4CO2(g)+6H2O(g)+1560.8kJ/mol
D、在101kPa下,甲烷的热值是891.0kJ/g
下列解释实验事实的化学方程式正确的是
| A.FeCl3溶液中通入SO2,溶液黄色褪去:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
B.90℃时,测得纯水中c(H+)·c(OH-)=3.8 ×10-13:H2O(l) H+(aq)+OH-(aq)△H<0 H+(aq)+OH-(aq)△H<0 |
| C.氨水中滴入酚酞溶液.溶液变红:NH3·H2O=NH4++OH- |
| D.向苯酚钠溶液中通入CO2,溶液变浑浊:2C6H5ONa+CO2+H2O→2C6H5OH+Na2CO3 |
在密闭容器中,一定条件下进行如下反应:NO(g)+CO(g)
 N2(g)+CO2(g)△H=-373.2KJ/mol,达到平衡后,为提高NO的转化率和该反应的速率,可采取的措施是
N2(g)+CO2(g)△H=-373.2KJ/mol,达到平衡后,为提高NO的转化率和该反应的速率,可采取的措施是
| A.加催化剂同时升高温度 |
| B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 |
| D.降低温度同时增大压强 |
下列关于①苯②乙醇③乙酸④葡萄糖等有机物的叙述中,不正确的是
| A.可用新制的氢氧化铜鉴别③与④ | B.只有③能与金属钠反应 |
| C.①、②、③均能发生取代反应 | D.一定条件下,④可以转化为② |
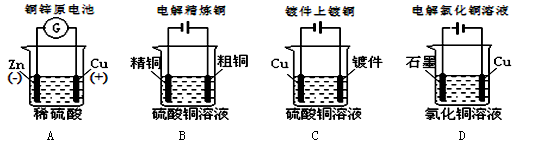
下列图示中关于铜电极的连接或描述错误的是