现有10种元素的性质、数据如下表所列,它们均为短周期元素。回答下列问题:
| |
A |
B |
C |
D |
E |
F |
G |
H |
I |
J |
| 原子半径(10-9m) |
0.074 |
0.160 |
0.152 |
0.110 |
0.099 |
0.186 |
0.075 |
0.082 |
0.102 |
0.037 |
| 最高或最低 化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
+6[ |
+1 |
| -2 |
|
|
-3 |
-1 |
|
-3 |
|
-2 |
|
(1)H的元素符号是 ; B在元素周期表中的位置是(周期、族)
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是 。
(3)化合物F2A2的电子式是: ,构成该物质的化学键类型为________________(填“离子键、极性键或非极性键”)
当F2A2与J2A的反应中有3.01×1023个电子转移时,参加反应的F2A2的质量是 g。
(4)用电子式表示J2A的形成过程: ;
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导与直流电源相连。请回答以下问题: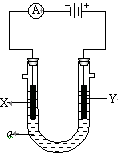
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则电解池中X极上的电极反应式为。
②检验该Y电极反应产物的方法是
③该反应的总反应方程式是:
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
① X电极电极反应式是,
② Y电极的材料是。
(8分)钢铁很容易生锈而被腐蚀。
(1)钢铁腐蚀主要是吸氧腐蚀,吸氧腐蚀过程中的电极反应为:
负极______________________________;
正极_______________________________。
(2)为了降低某水库的铁闸门的腐蚀速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用 _________(填序号)。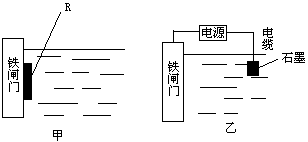
| A.铜 | B.钠 | C.锌 | D.石墨 |
(3)图乙所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的___________极上。
一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g) H2(g)+I2(g),H2物质的量随时间的变化如图所示。
H2(g)+I2(g),H2物质的量随时间的变化如图所示。
(1) 0—2 min内的平均反应速率v(HI)=。
该温度下,H2(g)+I2(g) 2HI(g)的平衡常数K=。
2HI(g)的平衡常数K=。
(2)相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则是原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数
2A B + C在某一温度时,达到平衡。
B + C在某一温度时,达到平衡。
(1)若温度升高,平衡向正反应方向移动,则正反应是___________反应(填放热或吸热);
(2)若B为固体,降低压强平衡向逆反应方向移动,则A呈___________态;
(3)若A是气态时,加压时,平衡不移动,则B为_________态,C为__________态;
(4) 若A、B、C均为气体,加入催化剂,平衡___________移动(填正向、逆向、不)
、(1)写出下列反应的热化学方程式
①1molN2 (g)与适量O2 (g)反应生成NO(g),需吸收68kJ的热量
②1g 硫粉在氧气中充分燃烧放出 9.36kJ热量
(2)氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
①若电解质溶液为KOH,其正极反应方程式为:
②若电解质溶液为硫酸,负极反应方程式为:。