某物质A的产量可以用来衡量一个国家的石油化工发展水平。其与水加成的产物B是一种常用的有机溶剂,在生活中有重要的应用。
(1) A的电子式为________,B的分子式为________。
若用B与O2制成燃料电池,并以稀硫酸溶液为电解质溶液,回答(2)-(5)题:
(2)负极上的电极反应式为_______________________________________。
(3)消耗标准状况下的5.6 L O2时,有__________mol电子发生转移。
(4)开始放电时,正极附近溶液的pH__________(填“增大”、“减小”或“不变”);
(5)溶液中H+由___________区向__________区移动(填“正极”或“负极”)。
将W g木炭与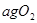 同时装入一个装有压力表体积不变的密闭容器中,压力表所示压强为
同时装入一个装有压力表体积不变的密闭容器中,压力表所示压强为 ,高温下容器中木炭与
,高温下容器中木炭与 均完全反应后恢复到原温度,压力表的示数为
均完全反应后恢复到原温度,压力表的示数为 ,试求:
,试求:
(1)当W取值发生变化时,反应后压强P也发生变化,P的最大值(以 表示)是______。
表示)是______。
(2)以W表示满足题设条件的a的取值范围__________。
(3)在题设条件下,W、a、P、 之间必须满足函数系W=f(a、
之间必须满足函数系W=f(a、 、P),写出该函数表达式:__________________。
、P),写出该函数表达式:__________________。
下表摘自国家环境监测中心公布的某时间我国部分大城市空气监测周报.
| 城市 |
污染 指数 |
首要 污染物 |
空气质 量级别 |
城市 |
污染 指数 |
首要 污染物 |
空气质 量级别 |
| 北京 |
92 |
TSP |
Ⅱ |
济南 |
76 |
TSP |
Ⅱ |
| 天津 |
82 |
TSP |
Ⅱ |
武汉 |
83 |
NOx |
Ⅱ |
| 长春 |
103 |
TSP |
Ⅲ |
深圳 |
77 |
NOx |
Ⅱ |
| 上海 |
74 |
NOx |
Ⅱ |
汕头 |
54 |
Ⅱ |
|
| 杭州 |
67 |
TSP |
Ⅱ |
成都 |
87 |
TSP |
Ⅱ |
| 福州 |
42 |
Ⅰ |
重庆 |
98 |
SO2 |
Ⅱ |
|
| 厦门 |
25 |
Ⅰ |
贵阳 |
69 |
TSP |
Ⅱ |
注:TSP:空气中飘尘;NOx:含氮氧化物.
阅读分析上表,回答下列问题:
(1)经济特区中,空气质量最好的城市是________,直辖市中空气质量最差的城市
是________.
(2)最容易出现酸雨的城市是________.为防止城市出现酸雨,降低煤燃烧时向大
气排放的SO2,工业上将生石灰或石灰石和含硫煤混合使用.请写出燃烧时,有
关“固硫”(不使含硫化合物进入大气)反应的化学方程式
___________________________________________________________________.
①②③④⑤五种元素,在元素周期表中的位置如图所示。回答下列问题: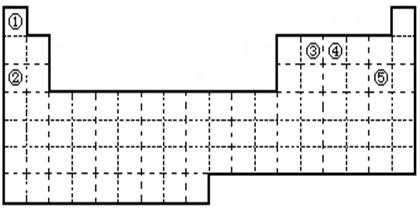
(1)①②③④⑤五种元素中,金属性最强的元素是 (写元素名称), 该元素的单质在空气中燃烧的化学方程式为 。
(2)元素②的最高价氧化物对应的水化物属于 化合物,(填“共价”或“离子” ),其电子式为 , 试比较②和③原子半径的大小
② ③(填“﹥” 或“﹤” )
(3)画出元素④的原子结构示意图 ,该元素的最高价氧化物的
水化物能与Cu发生反应,反应中作氧化剂的是(写化学式) 。
(4)写出元素⑤在周期表中的位置 ,以海水中含量最大的物质为原料可以生产⑤的单质,同时还可以得到另外两种重要的工业原料,该反应的化学方程式为 。
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外L层电子数是M层电子数的4倍。
①甲、乙元素分别为 、 (写元素名称)
②写出②的最高价氧化物对应的水化物与甲的最高价氧化物反应的离子方程式
工业上将磷酸钙、石英砂和炭粉混在电弧炉中焙烧来制取白磷:
Ca3(PO4)2+SiO2+C—CaSiO3+P4+CO↑
(1)配平以上方程式
Ca3(PO4)2+ SiO2+C=CaSiO3+P4+ CO↑
(2)已知白磷熔点为44.1℃,熔点280℃,据此判断其晶体类型属于
(3)有一种磷的结构式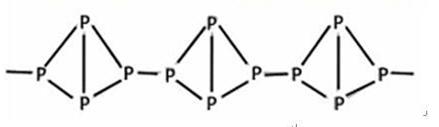 ,
,
有关它的叙述肯定不正确的是
| A.它在空气中完全燃烧的产物是P2O5 | B.它不溶于水 |
| C.它在常温下呈固态 | D.它与白磷互为同分异构体 |
NO分子因污染空气而臭名昭著。近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究热点,NO亦被称为“明星分子”。请回答下列问题:
(1)NO对环境的危害在于(填编号)
A.破坏臭氧层 B.光化学烟雾 C.造成酸雨
(2)下列关于NO的说法不正确的是
A.NO为无色气体
B.NO在空气中很不稳定
C.NO是汽车尾气的有害成分之一
D.NO分子所含电子总数为偶数
(3)在含Cu+离子的酶的活化中,亚硝酸根 (NO2—)离子可转化为NO ,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式