一定条件下,体积为10L的密闭容器中,1molX和1molY进行反应:
2X(g)+Y(g) Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是()
Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是()
| A.以X浓度变化表示的反应速率为0.001mol/(L·S) |
B.将容器体积变为20L,Z的平衡浓度变为原来的 |
| C.若增大压强,则物质Y的转化率减小 |
| D.若升高温度,X的体积分数增大,则该反应的△H>0 |
牙齿表面由一层硬的成分为Ca5(PO4)3OH的物质保护,它在唾液中存在下列平衡:
Ca5(PO4)3OH 5Ca2++3 PO43-+OH-。已知Ca5(PO4)3F(s)的溶解度比a5(PO4)3OH(s)更小,为了保护牙齿,世界各地均采用了不同的措施。以下措施中不能保护牙齿的是()
5Ca2++3 PO43-+OH-。已知Ca5(PO4)3F(s)的溶解度比a5(PO4)3OH(s)更小,为了保护牙齿,世界各地均采用了不同的措施。以下措施中不能保护牙齿的是()
| A.饮用纯净水 | B.在牙膏中添加适量的Ca2+或PO43-离子 |
| C.在饮用水中加入适量氟化物添加剂 | |
| D.在牙膏中加入氟化物添加剂 |
下列过程一定释放出能量的是()
| A.化合反应 | B.分解反应 | C.分子拆成原子 | D.原子组成分子 |
下列事实不能用勒沙特列原理解释的是()
| A.浓度均为0.1 mol·L-1的新制氯水,加入少量NaHSO3晶体,片刻后,溶液中HClO 分子的浓度减小 |
| B.室温下,将1 mL pH=3的醋酸溶液加水稀释至100 mL后,测得其pH<5 |
| C.在硫化氢水溶液中加入碱有利于S2—的生成 |
| D.500℃左右比室温更利于合成氨反应 |
1 mol某烃在氧气中充分燃烧,需要消耗氧气179.2 L(标准状况下)。它在光照的条件下与氯气反应能生成3种不同的一氯取代物。该烃的结构简式是()
A.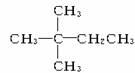 |
B.CH3CH2CH2CH2CH3 |
C.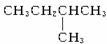 |
D.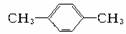 |