下列除去杂质的方法正确的是
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离。
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏。
③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶。
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
| A.①② | B.③④. | C.②④ | D.②③ |
常温下,将甲酸和氢氧化钠溶液混合,所得溶液 pH=7,则此溶液中
A C(HCOO-)>C(Na+) B C(HCOO-)<C(Na+)
C C(HCOO-)=C(Na+) D无法确定C(HCOO-)与C(Na+)的关系
某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A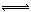 H++HA- HA-
H++HA- HA-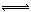 H++A2-;设有下列四种溶液:
H++A2-;设有下列四种溶液:
(1)0.01mol.L-1的H2A溶液
(2)0.01mol.L-1的NaHA溶液
(3)0.02mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(4)0.02mol.L-1的NaOH与0.02 mol.L-1的NaHA溶液等体积混合液
下列说法正确的是
AC(H+)最大的是(2) B C (A2-) 最小的是(2)
C C( H2A)最大的是(3) D C(HA-)最大的是(1)
将标准状况下的2.24 L CO2通入150 mL 1mol / LNaOH溶液中,下列说法正确的是
A.c( )略大于c( )略大于c( ) ) |
| B.该溶液只能与酸反应,不能与碱反应 |
C.c(Na+)等于c( )与c( )与c( )之和 )之和 |
D.c( )略小于c( )略小于c( ) ) |
对已达化学平衡的下列反应2X(g)+Y(g) 2Z(g);减小压强时,对反应产生的影响是
2Z(g);减小压强时,对反应产生的影响是
A逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C正、逆反应速率都减小,平衡向逆反应方向移动
D正、逆反应速率都增大,平衡向正反应方向移动
向某天然硬水中加入石灰,离子方程式正确但不能降低水的硬度的是
A 2Ca2++ 2HCO3-+2OH-=2CaCO3+2H2O
B 2Ca2+ + Mg2++ 2HCO3-+4OH-=2CaCO3+2H2O+Mg(OH)2
C 2OH-+ Mg2+= Mg(OH)2
D CaCO3+H2O+CO2 = Ca2++ 2HCO3-