氰酸(化学式:HOCN)是一种有挥发性和腐蚀性的液体,在水中立刻发生如下反应形成盐X(俗名碳铵):HOCN + 2H2O → X。
(1). 在上述反应所涉及的各元素中,半径最大的元素原子在周期表中的位置是___________,该原子核外电子共占据_______个轨道。
(2). X所含阳离子的电子式是________;已知25℃时0.1mol/L X溶液pH =7.8,用离子方程式表示原因:______________________。
(3). 能说明氮元素的非金属性比碳元素强的事实是_________(选填编号)。
a. 共用电子对偏向:H-N>H-C b. 氧化性:NO2>CO2
c. 酸性:HNO3>H2CO3 d. 沸点:NH3>CH4
(4). 据测定,氰酸有两种结构,一种分子内含有叁键,称为正氰酸,另一种分子内不含叁键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。请分别写出正氰酸和异氰酸的结构式:_______________、______________。
A是生产某新型工程塑料的基础原料之一,结构简式为: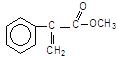
(1)写出A分子式的_____ ______
(2)拟从芳香烃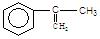 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下:
已知:A在酸性条件下水解生成有机物B和甲醇。
(a)写出⑤反应类型__________(b)写出H的结构简式__________
(c)已知F分子中含有“—CH2OH”,通过F不能有效、顺利地获得B,其原因是 ________
(d)两分子H之间发生反应生成六元环酯结构简式是:。
有机物A无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实验步骤 |
解释或实验结论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为:。 |
(2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现分 别增重5.4g和13.2g。 别增重5.4g和13.2g。 |
(2)A的分子式为:。 |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 |
(3)A中含有官能团的名称:。 |
(4)A的核磁共振氢谱如下图: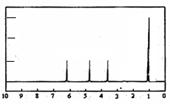 |
(4)A中含有种氢原子。 |
(5)综上所述,A的结构简式为:。 |
烃A完全燃烧生成的二氧化碳的物质的量比水的物质的量少,0. 1molA完全燃烧后的生成物全部被碱石灰吸收,使碱石灰增重26.6g。A的一溴取代产物有2种结构B1、B2。对B2进行核磁共振氢谱分析,只有一种吸收峰。请根据下图所示的各有机物之间的转化填空:
1molA完全燃烧后的生成物全部被碱石灰吸收,使碱石灰增重26.6g。A的一溴取代产物有2种结构B1、B2。对B2进行核磁共振氢谱分析,只有一种吸收峰。请根据下图所示的各有机物之间的转化填空: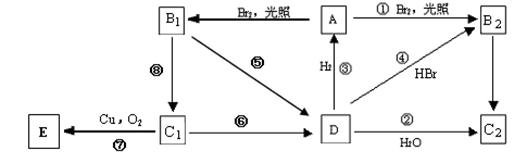
(1) 上述①~⑧反应中,属于取代反应的有_____,属于还原反应的是(填序号)。
上述①~⑧反应中,属于取代反应的有_____,属于还原反应的是(填序号)。
(2)物质C2的名称:
(3)写出①的化学方程式:
(4)写出⑤的化学方程式:
(5)D与某烷发生烷基化反应生成分子式为C 8H18的物质F,F的一卤代物只有4种,且碳链不对称。写出F的结构简式。
8H18的物质F,F的一卤代物只有4种,且碳链不对称。写出F的结构简式。
现有下列八种有机物:①乙烯、②甲苯、③溴乙烷、④乙醇、⑤苯酚、⑥乙醛、⑦乙酸、⑧乙酸乙酯。请回答:
(1)能跟银氨溶液发生银镜反应的是(填序号,下同)。
(2)能使氯化铁溶液变紫色的是。
(3)可以一步反应生成乙烯的是。
(4)能够与金属钠反应生成氢气的是。
(5)在一定条件下能跟新制氢氧化铜反应的是。
书写下列反应的化学方程式(有机物写结构简式)
(1)实验室制乙烯
(2)制取TNT
(3)由1,2—二溴乙烷制取乙二醇
(4)向浓溴水中滴加苯酚溶液
(5)3-甲基丁醛与新制氢氧化铜反应