某化学小组围绕燃烧与灭火的主题开展了相关活动。请你参与完成:
【知识回忆】可燃物燃烧的必备条件是 ;
【交流讨论】
(1)改进后的装置(如图二)与图一相比,其优点是 。欲使图二中的红磷着火,可将试管从水中取出并 后才能对试管加热;
(2)将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如图三所示),结果观察到了“水火相容”的奇观,则大试管所装气体可能是 ;
【综合应用】“水火不相容”是指水能灭火,其实水有时也可以“生火”,比如钾遇水会立刻着火,因为钾遇水生成H2和一种碱,该反应是 (填“吸热”或“放热”)反应,其反应化学方程式为 。
、阳阳同学利用改进的稀释浓硫酸的实验装置来完成一个趣味实验。他将一定质量的镁带放入装置中,向A中加入适量的稀盐酸。A的名称是,在发生化学反应的过程中,他能观察到的实验现象是;用理化知识解释他在“U”型管中观察到的现象的原因是
。
在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整。
【实验目的】铁生锈条件的探究。
【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象。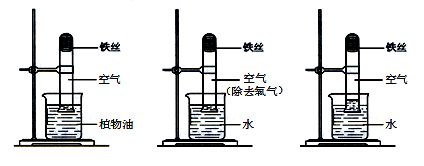
实验①实验②实验③
【实验现象】实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小。
【实验结论】铁生锈实际上是铁与空气中的(填名称)发生反应的结果。
【实验思考】
(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的。(2)该实验创新之处在于:可根据和
两种现象来判断铁丝反应进行的情况。
(3)用完的菜刀要擦干存放,理由是。
(4)铝比铁活泼,但铝难腐蚀,原因是。
物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变?小南、小岗按下面的步骤进行探究:
【提出假设】物质发生化学变化前后总质量不变。
【制定计划】小南设计的实验装置和选用药品如A所示,小岗设计的实验装置和选用药品如B所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察。
A B
【收集证据】小南在整个过程中观察到的现象是。
B中物质发生反应的化学方程式是。
【交流与评价】小南认为:在化学反应中,生成物的总质量与反应物的总质量相等;
小岗认为:在化学反应中,生成物总质量与反应物总质量不相等。
你认为的结论正确,导致另一个实验结论错误的原因是。
请从原子的角度分析你认为正确的结论的原因:。
【拓展与延伸】使用上述实验B装置,请你选择另外两种药品进行实验达到实验目的,这两种药品可以是和(填化学式)[注:以上四种药品均不能再用]
实验室制取氧气的实践与研究。
(1)过氧化氢是一种无色透明的无毒液体,过氧化氢溶液俗称“双氧水”,具有强氧化性。贮运过氧化氢的试剂箱上最适合粘贴的一张标识是____________(从上图中选填字母序号)。
(2)过氧化氢溶液常用于实验室制取氧气。可供选择的仪器或装置如下图所示。
①要收集干燥的氧气,整套装置的连接顺序为(由气体发生装置开始)_________(选填字母A~E);
②加入药品通常采用“把过氧化氢溶液缓缓加入盛有少量MnO2的反应容器中,优点是________________________________________________________;
③MnO2可以连续反应使用,理由是____________;
④写出该化学反应的文字表达式。
(3)任何物质都具有两面性,对物质的认识越深入,就越能充分、合理地利用物
质为人类服务,请从物质两面性的角度,说说你对氧气的认识(各举两例)。(本小题答对
奖励4分,但化学试卷总分不超过60分)
| 应用氧气 |
隔绝氧气 |
实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物,极易与空气中水蒸气和CO2反应而变质。同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究。
(1)【猜想】猜想Ⅰ:没有变质,“碱石灰”中只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和 Na2CO3
(2)【实验】如图所示:
实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热。
(3)【判断】
a.若Ca(OH)2、CaCO3和Na2CO3溶于水无明显的温度变化,则猜想Ⅱ______________; (填“成立”或“不成立”)
b.操作③发生反应的化学方程式为______________________________________;
由操作④的现象判断:滤液C中的溶质一定含有_______________(写化学式);
由此判断猜想Ⅰ_________(填“成立”或“不成立”)
c.综合a和b的结论,判断该样品变质情况为____________(填“全部变质”或“部分变质”)下列对样品成分的分析正确的是______(填序号)。
① 样品中一定含NaOH
② 样品中一定含Na2CO3
③ 样品中含NaOH、CaO中的一种或两种
【拓展】由上述实验说明,实验室中“碱石灰”应_______保存;操作②中玻璃棒的作用是 ___________________。