金属是现代生活和工业生产中应用极为普遍的一类材料。
(1)图A是金属的一个应用实例,利用了金属的_______性。图B是两块金属片相互刻划后,在纯铜片上有明显的划痕。该实验探究的目的是_________________________。
(2)已知在相同的条件下,金属的活动性越强,金属和酸反应产生气泡(氢气)的速度就越快。Al、Cu、Fe三种金属在稀盐酸里的反应现象如图所示。
①图中Y所代表的金属是 (填“Cu”或“Fe”);
②Al、Cu、Fe三种金属的活动性由强到弱的顺序为 ;
③铝是一种活泼金属,但常温下铝却有较强的抗腐蚀性,其原因是 ;
④将一片铝箔放到酒精灯火焰上加热,会发现熔化的铝并不滴落,好像有一层膜兜着。由此可知氧化铝的熔点 铝的熔点(填“>”或<”)。
(3)用一铝制易拉罐收集满一罐CO2气体,加入适量氢氧化钠溶液,封上口,振荡,会发现易拉罐先变瘪,过一段时间后又重新鼓起。
①拉罐变瘪的原因是(用化学方程式表示) 。
②易拉罐为什么又重新鼓起呢?原来铝是一种特殊的金属,能和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和一种气体单质。已知:在一个化学反应中,如果有元素化合价的升高,必然有元素化合价的降低。则铝和氢氧化钠溶液反应生成的气体单质是
(4)下图是工业炼铁的基本生产流程示意图。请回答下列问题:
①写出设备A 的名称: ;
②写出以赤铁矿为原料在高温下制取铁的化学方程式: ;
③除了上面的炼铁方法之外,还可用铝热法炼铁,即用铝在高温下把氧化铁中铁置换出来,写出该反应的化学方程式 。
化学与社会密切相关, 从化学的视角认识厨房中蕴含的丰富化学知识。
(1)下列食物中富含维生素的是(填字母序号,下同);青少年正处于生长发育期,需要摄取较多的蛋白质。如图中蛋白质含量最高的是。
(2)为了全民的健康,我国推广使用强化铁酱油,这里的“铁”指的是(填“单质”、“元素”或“原子”)。
(3)许多家庭做饭用罐装的“煤气”作燃料,罐中所装的是液化石油气。
①它是石油化工的一种产品。石油属于能源(填“可再生”或“不可再生”)。
②若厨房失火时,移走“煤气罐”,这是利用了原理灭火(填序号)。
A.清除可燃物
B.使可燃物与氧气隔绝
C.降低可燃物的着火点
用化学用语表示:
(1)磷元素;
(2)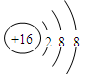 表示的粒子___________;
表示的粒子___________;
(3)+2价的钙元素;
(4)2个二氧化硫分子;
(5)碳酸根离子。
下图是氧气的制取与性质实验装置图。
回答下列问题:
(1)装置B的作用是,装置C中硫粉燃烧的现象是,装置D的作用是。
(2)装置A中发生反应的化学方程式为,装置D中发生反应的化学方程式为。
元素周期表中某元素的原子结构示意图如下:
(1)上述结构图中的
=。
(2)硅原子的结构示意图为: 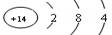
上图中与其化学性质相似的元素是(填元素符号)。
(3)根据图示信息,确定一个水分子中所含电子总数为。
观察下图并回答问题:
由上图可知,HCl与NaOH的反应实质是H+和OH-之间的反应,此反应可表示为:H++0H-=H2O。像这种用实际参与反应的离子来表示反应的式子称为离子方程式。任何复分解反应都可用离子方程式来表示。
[练习] 按照书写化学方程式的要求写出下列反应的离子方程式
HCl溶液与AgNO3溶液反应:。
HNO3溶液与Na2CO3溶液反应:。
[归纳] 复分解反应的实质是:阴阳离子结合生成的反应。
[应用] 判断在水溶液中一定能大量共存的离子组是。
a、Na+、H+、Cl-、CO32-b、H+、Ba2+、Cl-、SO42-
c、Cu2+、Na+、NO3-、OH-d、H+、K+、Cl-、SO42-