航天技术使用氢氧电池具有高能、轻便,不污染优点,氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式均可表示为:2H2+O2 = 2H2O ,酸式氢燃料电池的电解质是酸、其负极反应为:2H2-4e-= 4H+,则正极反应为 ;碱式氢氧燃料电池的电解质是碱,其正极反应表示为:O2+2H2O+4e-= 4OH-,则负极反应为: 。
高分子化合物A和B的部分结构如下: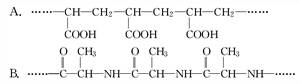
(1)合成高分子化合物A的单体是________,生成A的反应是________反应.
(2)合成高分子化合物B的单体是________,生成B的反应是________反应.
完成下列反应的化学方程式,并指出反应类型.
(1)由乙烯制取聚乙烯:
________________________________________________________________________,
(2)由丙烯制取聚丙烯:
________________________________________________________________________,
(3)由对苯二甲酸(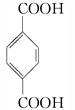 )与乙二醇发生反应生成高分子化合物:
)与乙二醇发生反应生成高分子化合物:
______________________________________,________________________.
聚苯乙烯的结构为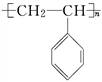 ,试回答下列问题:
,试回答下列问题:
(1)聚苯乙烯的链节是________________________,单体是______________________.
(2)实验测得某聚苯乙烯的相对分子质量(平均值)为52000,则该高聚物的聚合度n为________________.
含有氨基(—NH2)的化合物通常能够与盐酸反应,生成盐酸盐,如:R—NH2+HCl―→R—NH2·HCl(R代表烷基、苯基等).
现有两种化合物A和B,它们互为同分异构体.已知:
①它们都是对位二取代苯;
②它们的相对分子质量都是137;
③A既能被NaOH溶液中和,又可以跟盐酸成盐,但不能与FeCl3溶液发生显色反应;B既不能被NaOH溶液中和,也不能跟盐酸成盐;
④它们的组成元素只可能是C、H、O、N、Cl中的几种.
请按要求填空:
(1)A和B的分子式是________.
(2)A的结构简式是______________________;
B的结构简式是______________________.
下图是以C7H8为原料合成某聚酰胺类物质(C7H5NO)n的流程图.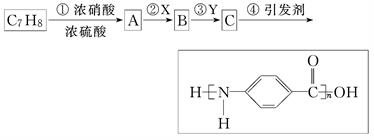
回答下列问题:
(1)聚酰胺类物质所具有的结构特征是________.(用结构简式表示)
(2)反应①通常应控制的温度为30℃左右,在实际生产过程中应给反应体系加热还是降温?为什么?____________________________________________________.若该反应在100℃条件下进行,则其化学反应方程式为_________________________________.
(3)反应②和反应③从氧化还原反应的角度看是________基团被氧化为________基团,________基团被还原为________基团.从反应的顺序看,应先发生氧化反应还是还原反应?为什么?_______________________________________________________________
_______________________.