.(12分)某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,某同学设计如下试验:
(1)取样品 ag ,称取时使用的仪器名称为 。
(2)将样品溶于足量的稀盐酸中,过滤,滤渣中含有 ,在溶解过滤时使用的玻璃仪
器有 。
(3)往滤液中加入过量的NaOH溶液、过滤,写出该步操作中有关的离子方程式 。
(4)在第( 3 )步的滤液中通入足量CO2,过滤。有关反应的离子方程式是 。
(5)步骤(4)过滤后的滤渣用蒸馏水洗涤数次后,烘干并灼烧至质量不再减轻为止,冷却后称量,质量为bg,则原样品中铝的质量分数是 。
(6)若步骤(3)中加入氢氧化钠的量不足,则实验结果偏 (填“高”、“低”或“不影响”,下同);若步骤(5)中滤渣没有洗涤,则实验结果偏 ;若滤渣燃烧不充分,则实验结果偏 。
某实验需要用到80mL 1.5 mol/L稀H2SO4溶液,现用18.4mol/L的浓硫酸
(ρ=1.84g·cm-3)进行配制。
(1)所需浓硫酸最小体积为_________。
(2)量取所需浓H2SO4,应选用__________mL量筒。(填5、10或50)
(3)稀释浓H2SO4的方法(简要操作)_____________________________。
(4)容量瓶使用前,检验其是否漏水的方法是_________________。
(5)稀释后的浓H2SO4若立即转移至容量瓶中,所配溶液的浓度将____________。(填偏大、偏小或不变)
(6)定容时俯视刻线,所配溶液的浓度将。(填偏大、偏小或不变)
某化学课外小组用海带为原料制取少量碘水。现用四氯化碳从碘水中萃取碘并用分液漏斗分离两种溶液。其实验操作可分为如下几步:
| A.把盛有溶液的分液漏斗放在铁架台的铁圈中 |
| B.把50mL碘水和15mL CCl4加入分液漏斗中,并盖好玻璃塞 |
| C.检验分液漏斗活塞和上口的玻璃塞是否漏水 |
| D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把漏斗放正 |
(E)旋开活塞,用烧杯接收溶液
(F)从分液漏斗上口倒出上层水溶液
(G)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔
(H)静置,分层
(1)上述操作的正确顺序的代号
(2)上述(G)步骤操作的目的是
(3)能否用汽油代替CCl4,原因是
配制500mL 1.0mol·L—1的NaOH溶液时,下列哪些操作会使实验结果偏高_____________;偏低__________;无影响______________。
| A.称量时,直接把氢氧化钠放在纸上称量,且称量时间过长 |
| B.称量时,固体放在右盘,砝码放在左盘 |
| C.称量时所用砝码生锈 |
| D.原容量瓶用蒸馏水洗净后未干燥 |
E . 移液后,未洗涤烧杯和玻璃棒
F. 定容时,俯视刻度线
G. 颠倒摇匀溶液后,发现液面低于刻度线,再补加水到刻度线
H. 溶液尚未冷却到室温就注入容量瓶进行定容
二次合金中含有金、银、铂、钯等贵重金属,实验室以二次合金为原料提取金、银、铂、钯等贵重金属的步骤如下,试回答下列问题:
(1)浓硫酸浸煮过程中产生尾气的主要成分是(填写代号,下同),欲对该气体进行检验,最好的试剂是;
| A.H2 | B.SO2 | C.灼热的氧化铜粉末 | D.品红试剂 |
(2)操作Ⅰ的实验名称是,完成该实验需要的玻璃仪器有
(填写仪器名称);
(3)实验室制备的Cl2中混有水蒸气和HCl杂质,甲同学设计了如下图所示的实验装置来证明水蒸气和HCl杂质的存在,请根据甲同学的设计意图完成下列有关问题。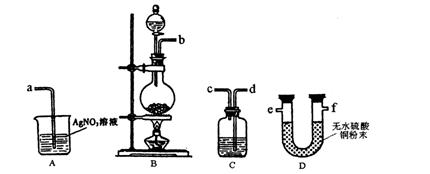
①各实验装置的接口顺序为:b接,接,接a;
②装置C的作用是;
③乙同学认为甲同学的实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加装置E。你认为装置E应加在之间(填装置序号),并且在广口瓶中放入(填写所用试剂或用品名称)。
实验室常利用甲醛法(HCHO)测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
4NH4+ +6HCHO =3H++6H2O+(CH2)6N4H+ [滴定时,1 mol (CH2)6N4H+消耗NaOH与 l mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤I称取样品1.500 g。
步骤II将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤III移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤III填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积________________(填“偏大”、“偏小”或“无影响”)
③滴定时边滴边摇动锥形瓶,眼睛应观察____________
(A)滴定管内液面的变化 (B)锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由_________色变成_________色。
(2)滴定结果如下表所示:
| 滴定 次数 |
待测溶液的体积 /mL |
标准溶液的体积/mL |
|
| 滴定前刻度 |
滴定后刻度 |
||
| 1 |
25.00 |
1.02 |
21.03 |
| 2 |
25.00 |
2.00 |
21.99 |
| 3 |
25.00 |
0.20 |
20.20 |
滴定时消耗NaOH标准溶液的体积的平均值V="__________mL;" 若NaOH标准溶液的浓度为0.1010 mol·L-1,则250 mL溶液中的n(NH4+)=__________mol,该样品中氮的质量分数为______。