如图所示,y表示沉淀的质量,x表示加入试剂的体积,能够用该图表示的反应是: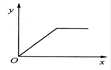
| A.向AlCl3溶液中加入浓氨水至过量 |
| B.向Ca(OH) 2溶液中通入CO2至过量 |
| C.向Na[Al(OH)4]溶液中加入盐酸至过量 |
| D.向AlCl3溶液中加入NaOH溶液至过量 |
铁和氧化铁的混合物共amol,加盐酸后固体全部溶解,共收集到bmol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则混合物中铁的物质的量为
A.1/2(a+b)mol B.(a-b)molC.1/2(a-b)mol C.(a+b)mol
向三份同浓度的25mL盐酸中分别加入质量不等的NaHCO3、KHCO3的混合物,测得产生
气体的体积如下表所示(不考虑气体溶解)
| 编号 |
1 |
2 |
3 |
| m(混合物)/g |
4.6 |
7.2 |
7.9 |
| V(CO2)(标准状况)/L |
1.12 |
1.68 |
1.68 |
下列分析推理正确的是
A.根据实验1中的数据可以计算出盐酸的浓度
B.混合物中NaHCO3的质量分数约为45.7%
C.根据第2、3组数据可以分析出第2组中的混合物完全反应
D.盐酸的物质的量浓度为1.5mol.L-1
25℃时,向浓度均为0.1mol.L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液,表示生成Al(OH)3的物质的量与加入的NaOH溶液的体积的关系如下图所示(已知当离子浓度小于1×10-5mol.L-1时为沉淀完全)。则下列说法与判断合理的是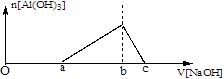
| A.25℃时,Fe(OH)3的溶解度大于Al(OH)3的溶解度 |
| B.25℃时,Fe(OH)3的溶度积大于Al(OH)3的溶度积 |
| C.当生成的Al(OH)3恰好完全溶解时,溶液中的溶质只有NaAlO2 |
| D.图中2a=b=6(c-b) |
将amol小苏打和bmol过氧化钠置于某体积可变的密闭容器中充分加热,反应后测得容器内的氧气为1mol,下列说法正确的是
| A.b=2 |
| B.反应中转移的电子数一定为2NA |
| C.容器中一定没有残余的CO2和水蒸气 |
| D.a:b≥1 |
一种新型镁铝合金的化学式为Mg17Al12,它具有储氢性能,该合金在一定条件下完全吸氢的化学方程式为:Mg17Al12+17H2=17MgH2+12Al,得到的混合物Y(17MgH2+12Al)在一定条件下能释放出氢气。下列说法正确的是
| A.该合金的熔点介于金属镁和金属铝熔点之间 |
| B.该合金中镁元素呈负价,铝元素呈正价 |
| C.制备该合金应在氮气保护下,将一定比例的Mg、Al单质在一定温度下熔炼而获得 |
| D.1mol Mg17Al12完全吸氢后得到的混合物Y与盐酸完全反应释放出H2,若消耗盐酸的体积为14L,则该盐酸的物质的量浓度为5mol.L-1 |