下列关于碱金属的原子结构和性质的叙述中不正确的是
| A.都能与水反应生成碱 | B.都是强还原剂 |
| C.都能在O2中燃烧生成过氧化物 | D.碱金属原子最外层都只有一个电子 |
根据下列实验事实:
(1)X+Y2+ X2++Y
X2++Y
(2)Z+2H2O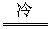 Z(OH)2+H2↑
Z(OH)2+H2↑
(3)Z2+的氧化性比X2+弱
(4)由Y、W作电极组成的原电池反应为:Y-2e- Y2+。
Y2+。
由此可知,X、Y、Z、W的还原性由强到弱的顺序是()
| A.X>Y>Z>W | B.Y>X>W>Z |
| C.Z>X>Y>W | D.Z>Y>X>W |
下列说法正确的是()
| A.钢铁因含杂质而容易发生电化腐蚀,所以合金都不耐腐蚀 |
| B.原电池反应是导致金属腐蚀的主要原因,故不能用来减缓金属的腐蚀 |
| C.钢铁电化腐蚀的两种类型主要区别在于水膜的pH不同,引起的正极反应不同 |
| D.无论哪种类型的腐蚀,其实质都是金属被氧化 |
X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X与Y组成原电池时,Y为电池的负极。X、Y、Z三种金属的活动性顺序为
| A.X>Y>Z | B.X>Z>Y | C.Y>X>Z | D.Y>Z>X |
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4Al+3O2+6H2O=4Al(OH)3,下列说法不正确的是( )
| A.正极反应式为:O2+2H2O+4e-=4OH- |
| B.电池工作时,电流由铝电极沿导线流向铂电极 |
| C.以网状的铂为正极,可增大与氧气的接触面积 |
| D.该电池通常只需要换铝板就可以继续使用 |
如下图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细。由此判断表中所列M、N、P物质,其中可以成立的是()
| M |
N |
P |
|
| A |
Zn |
Cu |
稀H2SO4溶液 |
| B |
Cu |
Fe |
稀HCl溶液 |
| C |
Ag |
Zn |
AgNO3溶液 |
| D |
Zn |
Fe |
Fe(NO3)3溶液 |