生活中的金属材料多数属于合金。下表列出了一些常见合金的主要成分和性能。
| 合金 |
合金的主要性能 |
主要成分及纯金属的性能 |
| 焊锡 |
熔点183℃ |
锡:熔点232℃;铅:熔点327℃ |
| 硬铝 |
硬度好 |
铝、铜、镁等,硬度小 |
| 不锈钢 |
抗腐蚀性好 |
铁、碳、铬、镍等,纯铁抗腐蚀性不如不锈钢。 |
(1)由上表可以推断,与组成合金的纯金属相比、合金的优点一般有 、 ;
(2)把硬铝放在足量的盐酸中,最后剩余的金属是 ,写出发生反应的其中一个化学方程式 ;该反应的基本类型属于 反应。
(3)铁制品暴露在空气中会发生锈蚀,而在铁中熔合了一定量的碳、铬、镍等形成不锈钢后,改变了纯铁的 ,因而其抗锈蚀性能比纯铁好得多。
金属材料的应用非常广泛。运用所学知识回答以下问题:
(1)铝制品比铁制品有更好的抗腐蚀性能,原因是铝的表面能生成一层,阻止铝的进一步氧化。
(2)铜可以拉成铜丝,这是利用了金属的。
(3)锰(Mn)钢属于铁合金,可用于制造钢轨。取少量的锰钢碎屑加入盛有足量稀盐酸的烧杯中,充分反应后烧杯底部剩有固体,该固体中一定含有。
(4)将一定量的锌粉放入稀盐酸、氯化亚铁、氯化铜的混合溶液中,充分反应后过滤,再向滤渣中加盐酸有气泡产生。则滤渣中一定含有的固体是;滤液中一定不含的物质是。
化学与生产生活息息相关,请运用化学知识回答以下问题:
(1)为了使我们爱吃的酸菜长期保存,一般是将酸菜放在陶罐中,盖上盖后,再在盖的周围放适量的水,这样做的目的是以防酸菜变质。
(2)工业上用盐酸去铁锈(用化学方程式表示)。
(3)工业上用磁铁矿石炼铁(用化学方程式表示)。
(4)用醋酸除水垢(主要成分CaCO3)(用化学方程式表示)。
(5)硫酸铵不能与熟石灰混合施用,原因是(用化学方程式表示)。
化学是以实验为基础的学科,根据实验1、实验2回答下列问题: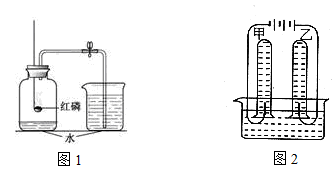
(1)实验1的实验目的是。
(2)实验1中发生化学反应的化学方程式是。
(3)实验1在冷却至室温后打开弹簧夹,发现进入集气瓶内的水少于瓶内空气体积的1/5体积,原因可能是(答一条即可)。
(4)实验2是电解水的简易装置图,电解一段时间后,甲试管中的气体体积比乙试管中的气体体积(填“多”或“少”)。
(5)实验2说明水是由组成的。
结合下图所示实验装置回答问题: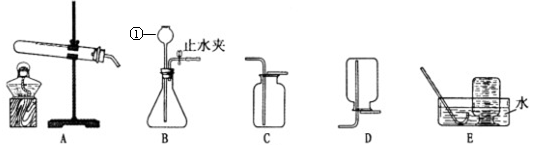
(1)仪器①的名称是_______。
(2)实验室制取二氧化碳,选用的发生装置是,反应的化学方程式为
(3)实验室若用高锰酸钾制取较纯净的氧气,反应的化学方程式为,应选用的收集装置是(填标号),若观察到____________________,说明瓶中已充满氧气。
(5分)应用所学知识,回答下列有关金属的问题:
(1)人体中含量最多的金属元素是(用元素符号回答);
(2)生活中常用铜丝作导线,主要是利用铜的性;
(3)字母A、B、C、D表示金属活动性顺序表中常见的四种金属。
已知:①A+BSO4=ASO4+B
②C+H2SO4=CSO4+H2↑
③B+2DNO3=B(NO3)2+2D
根据上述反应能判断出其中三种金属的活动性顺序,其金属活动性由强到弱的顺序是(填字母)
(4)向FeCl2和CuCl2的混合溶液中加入一定质量的锌粉充分反应后过滤,向滤渣中加入稀盐酸有气泡产生,则滤渣中含有的物质是或。