下图是工业生产纯碱的工艺流程示意图。
已知:①粗盐水中含有MgCl2、CaCl2;②常温下,NH3极易溶于水,CO2能溶于水,③NaHCO3加热易分解,Na2CO3加热不易分解。
完成下列填空:
(1)粗盐水加入沉淀剂NaOH、Na2CO3分别除去MgCl2、CaCl2,固体C为 ,书写其中一个反应的化学方程式 ;
(2)在工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是 ,“碳酸化”时,NaCl、NH3、CO2和H2O相互作用析出NaHCO3,写出该反应的化学方程式 。
(3)“碳酸化”后过滤获得的NH4Cl可用作 肥,也可先 (填“加热”或“冷却”)NH4Cl溶液,再加入石灰水以循环使用的物质是 ;
(4)“煅烧”时,NaHCO3分解生成的气体D是 ,若将气体D直接排入空气不合理的理由是 。
(5)鉴别产品纯碱中是否含有碳酸氢钠的方法是 。
已知A、B、C、D、E是 初中化学中常见的五种物质。其中A、D是黑色固体,B、C、E是无色气体,B的相对分子质量小于气体C,化合物D中含有金属元素,该金属元素的单质是世界年产量最高的金属。它们在一定条件下的转化关系如右图所示(→表示转化)。请回答下列问题:
(1)A物质是;
(2)评价物质B的“利”与“弊”(各写一例)
利:;
弊:。
(3)写出E转化为D的化学方程式:。
图中,甲是铁的氧化物,其中铁元素质量分数为70%;乙是黑色粉末;丙和丁是可溶性盐。若试剂A是稀盐酸,则A与甲反应的化学方程式为;试剂B中含有钠元素,则该试剂是(填化学式)溶液,丙与试剂B反应的化学方程式为;反应③的发生需要氧气和水,其化学方程式。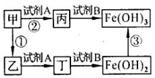
有一瓶气体,它由H2、CO2、CO、CH4中的一种或几种组成。用它进行以下实验:
(1)将气体通入过量的澄清的石灰水,未见石灰水浑浊。
(2)在导管口将气体点燃,气体安静的燃烧,火焰呈蓝色。用一个冷而干燥的烧杯罩在火焰上,烧杯内壁上出现水珠,把烧杯迅速倒转过来,注入少量澄清的石灰水,石灰水变浑浊。
用化学式填空回答问题:
(3)气体中一定没有。
(4)气体的组成可能是(有几种可能就填几种,可以不填满)
①②③④⑤⑥
在下面关系图中,A、B、C、D是初中化学中常见的单质,甲、乙分别是甲烷充分燃烧时产生的两种物质,丁是常用建筑材料的主要成分,G为无色有刺激性气味的气体,能使湿润的紫色石蕊试纸变蓝,J是赤铁矿的主要成分。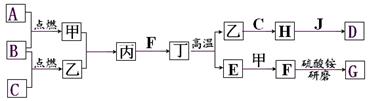
(1)写出化学式:甲是,G是。
(2)写出F与硫酸铵反应的化学方程式:。
A~I是初中化学常见的物质,图中“→”表示转化关系,“——”表示相互可以发生反应(部分物质和反应条件未标出)。F是天然气的主要成分,A、B、G、H是氧化物,C、I是单质,D、E中含有三种元素,D能使紫色石蕊变红色。请回答下列问题: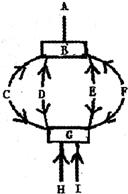
(1)D的化学式是:;
(2)请写出C的一种用途:;
(3)写出H转变为G的化学方程式:;
(4)A与B反应的基本反应类型是。