1mol某烃能与2mol HCl完全加成,其产物最多能被8mol Cl2完全取代,则原烃可能为( )
| A.乙炔 | B.环丁烯 | C.1一丙炔 | D.1,3一丁二烯 |
有机物A的结构简式为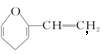 A的同分异构体中含苯环的化合物共有
A的同分异构体中含苯环的化合物共有
| A.3种 | B.4种 | C.5种 | D.6种 |
由2-氯丙烷制取少量的1,2-丙二醇时,需要经过下列哪几步反应
| A.加成→消去→取代 | B.消去→加成→水解 |
| C.取代→消去→加成 | D.消去→加成→消去 |
白藜芦醇广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性。能够跟1mol该化合物起反应的Br2或H2的最大用量分别是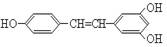
| A.1mol 1mol | B.3.5mol 7mol |
| C.3.5mol 6mol | D.6mol 7mol |
下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比为3∶1的是
分子式为C4H10O的醇催化氧化后能生成的醛有
| A.2种 | B.3种 | C.4种 | D.5种 |