( 7分 )同一周期的主族元素,从左到右,原子半径逐渐 ,得电子能力逐渐______,非金属性逐渐______;同一主族元素,从上到下原子半径逐渐 ,失电子能力逐渐______,单质的还原性逐渐______,氧化性逐渐______。
某温度(t℃)时,水的KW=10-13,则该温度(填大于、等于或小于)______25℃,理由是_________________________________________________,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,
(1)若所得混合溶液为中性,则a:b=_________;
(2)若所得混合溶液pH=2,则a:b=__________。
下图表示的是N2 + 3H2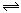 2NH3;△H<0达到平衡后,改变条件建立的新平衡(图中横坐标表示反应时间, 纵坐标表示反应速率)
2NH3;△H<0达到平衡后,改变条件建立的新平衡(图中横坐标表示反应时间, 纵坐标表示反应速率) 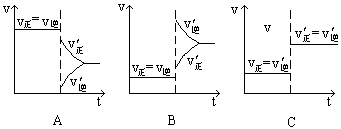
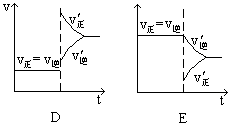
(1)表示减少H2的量而建立新平衡的是。
(2)表示压缩气体, 体积减小而建立新平衡的是。
(3)表示降低温度而建立新平衡的是。
(4)表示升高温度而建立新平衡的是。
(5)表示加入催化剂后而建立新平衡的是。
已知电子工业上常用FeCl3溶液来溶解电路板中的铜。某一反应体系有反应物和生成物共三种物质:FeCl3、FeCl2、Fe。完成下列问题:
(1)该反应中的还原产物的化学式是,氧化产物的化学式是。
(2)该反应中,发生还原反应的过程是(填化学式)→。
(3)该反应的离子方程式为:。
(4)标出该反应电子转移的方向和数目
(5)如反应转移了0.3mol电子,则(填“溶解”或“生成”)的铁的质量为。
有A、B、C、D四种盐,组成它们的阳离子有:Ba2+、Ag+、Na+、Cu2+中,阴离子有:NO3-、Cl-、SO42-、CO32-。某同学设计实验对它们进行鉴别:
⑴ 把四种盐分别溶解于盛有蒸馏水的四支试管中,均得到澄清溶液。通过观察及分析,该同学得出如下结论:
①可以确定的是A,则A为:(填化学式,下同);
②另三盐分别是:、 、,但不知道分别对应哪种物质。
⑵ 再向未确定的三支试管中分别加入盐酸,则B盐溶液有沉淀产生,C盐溶液有无色无味气体产生。该同学确定另三种盐的化学式分别为:
B_____________,C_____________,D_______________。
⑶ 请你帮该同学完成下列反应的离子方程式:
B+盐酸:
C+盐酸:
A与D混合:
验需要0.1mol/LNaOH溶液450mL,根据溶液配制中情况回答下列问题:
⑴ 实验中不需要的仪器有:
A.托盘天平 B. 烧杯 C. 500 mL容量瓶 D.玻璃棒 E.滴管 F.铁架台 G.烧瓶 H.酒精灯
⑵ 根据计算得知,所需NaOH的质量为g
⑶ 下列操作对所配浓度有何影响(填写字母)
偏大的有;偏小的有;无影响的有。
A、称量时用了生锈的砝码;
B、将NaOH放在纸张上称量;
C、NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中;
D、往容量瓶转移时,有少量液体溅出
E、未洗涤溶解NaOH的烧杯
F、定容时仰视刻度线
G、定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,不再加水。
H、容量瓶底部未干燥即用来配制溶液